��Ŀ����
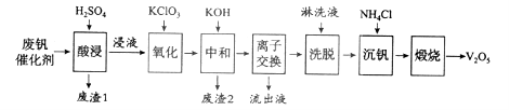
����Ŀ���ܼ��仯�����ڹ�ҵ�����ù㷺����ij��ҵ�������Ʊ������ܵĹ�ҵ������ͼ��
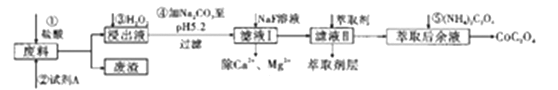
��֪���ٷ�������Ҫ�������������ܡ�������F2O3��Al2O3��MnO��CaO��SiO2�ȣ�
�ڽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
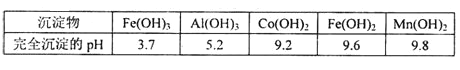
(1)�ڽ��������м���Co2O3�����ᷴӦ�������壬�˷�Ӧ�����ӷ���ʽΪ___________________ ��ʵ�����м��������ķ�����________________��
(2)�����Լ�A��Ŀ����_________________����������Ҫ�ɷ���_______________���ڽ���Һ���ȼ���˫��ˮ��Ӧ���ټ���̼���Ƶ�ԭ����(�������ӷ���ʽ�ͱ�Ҫ�����ּ�������)___________��
(3)��ȡ����Һ�м���(NH4)2C2O4����Co2+���ж�Co2+������ȫ�IJ�����____________________��
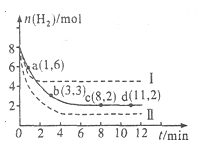
(4)��ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ����ͼ��ʾ������ҺII��������ȡ��pHΪ_____(�����)
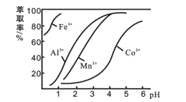
A.�ӽ�2.0 B. �ӽ�3.0 C. �ӽ�5.0
(5)�ڿ����м���CoC2O4���壬���ⶨ��210�桫290��Ĺ�����ֻ����CO2��һ�ֻ�����û���������Ԫ�ص���������Ϊ73.44%���˹��̷�����Ӧ�Ļ�ѧ����ʽ��________________________��
���𰸡�Co2O3+6H++2Cl��=2Co2++Cl2��+3H2O��ʪ��ĵ��۵⻯����ֽ����ȷ��Co3+��ȫ����ԭ��Co2+SiO2��Fe2+����ΪFe3+���ټ����̼���ƣ���![]() ����H+��Ӧ��
����H+��Ӧ��![]() ���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O
���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O![]() R(OH)3+3H+�����ƶ�����������������������ú����ϲ���Һ������(NH4)2C2O4�������������B3CoC2O4+2O2
R(OH)3+3H+�����ƶ�����������������������ú����ϲ���Һ������(NH4)2C2O4�������������B3CoC2O4+2O2![]() Co3O4+6CO2
Co3O4+6CO2
��������
(1)�ڽ��������м���Co2O3�����ᷴӦ����CoCl2��Cl2��������Ӧ�����ӷ���ʽΪCo2O3+6H++2Cl��=2Co2++Cl2��+3H2O��ʵ����ͨ����ʪ��ĵ��۵⻯����ֽ���飬����ֽ����ɫ����֤��������Ϊ������
(2)������Լ�AӦ����Fe����Ŀ����Ϊ��ȷ��Co3+��ȫ����ԭ��Co2+�������к���SiO2������ϡ���ᣬ���÷�������Ҫ�ɷ���SiO2���ڽ���Һ���ȼ���˫��ˮ��Ӧ��ʹ��Һ�е�Fe2+��ȫ����ΪFe3+���ټ����̼���ƣ���CO32-����H+��Ӧ�� c(H+)���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O![]() R(OH)3+3H+�����ƶ����������������������
R(OH)3+3H+�����ƶ����������������������
(3)��ȡ����Һ�м���(NH4)2C2O4����Co2+�������ú����ϲ���Һ������(NH4)2C2O4������������ֿ��ж�Co2+������
(4)��ͼʾ��֪����ҺpH=3����ʱ��Fe3+��Al3+��Mn2+����ȡ����ߣ���Co2+����ȡ�ʽϵͣ��ʴ�ΪB��
��5���û�������Co����������Ϊ73.44%����Co�UO��ԭ�Ӹ�����Ϊ![]() =3�U4����û�����Ļ�ѧʽΪCo3O4���ʷ���ʽΪ3CoC2O4+2O2_
=3�U4����û�����Ļ�ѧʽΪCo3O4���ʷ���ʽΪ3CoC2O4+2O2_![]() Co3O4+6CO2��
Co3O4+6CO2��

 ������������ϵ�д�
������������ϵ�д�