题目内容
【题目】
以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
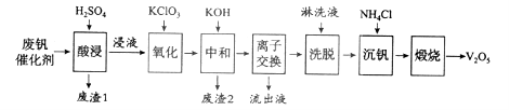
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
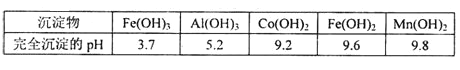
【答案】(1)V2O5+2H+=2VO2++H2O;SiO2;(2)0.5;(3)Fe(OH)3、Al(OH)3;
(4)碱;(5)K+ ;(6)2NH4VO3![]() V2O5+H2O+2NH3↑。
V2O5+H2O+2NH3↑。
【解析】(1)“酸浸”时V2O5转化为VO2+,V元素化合价不变,说明不是氧化还原反应,根据原子守恒可知反应的离子方程式为V2O5+2H+=2VO2++H2O;二氧化硅与酸不反应,则“废渣1”的主要成分是二氧化硅。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,V元素化合价从+4价升高到+5价,而氧化剂KClO3中氯元素化合价从+5价降低到-1价,则根据电子得失守恒可知需要氯酸钾的物质的量为3 mol÷6=0.5 mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中,同时生成氢氧化铁、氢氧化铝沉淀,则“废渣2”中含有Fe(OH)3、Al(OH)3。
(4)根据方程式可知为了提高洗脱效率,反应应该向逆反应方向进行,因此淋洗液应该呈碱性。
(5)由于前面加入了氯酸钾和氢氧化钾,则“流出液”中阳离子最多的是钾离子。
(6)根据原子守恒可知偏钒酸铵(NH4VO3)“煅烧”生成七氧化二钒、氨气和水,发生反应的化学方程式为2NH4VO3![]() V2O5+H2O+2NH3↑。
V2O5+H2O+2NH3↑。