题目内容
【题目】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H
2N2(g) +6H2O(g) △H
(1)
化学键 | H—O | O=O | N≡N | N—H |
键能kJ·molˉ1 | 463 | 496 | 942 | 391 |
△H=__________________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是__________________。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内![]() =1时,说明反应已达平衡
=1时,说明反应已达平衡
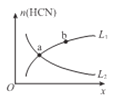
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
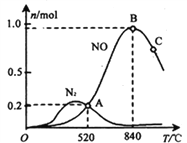
①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
② 520℃时,4NH3(g)+5O2![]() 4NO(g) +6H2O(g)的平衡常数K=____________________________ (不要求得出计算结果,只需列出数字计算式)。
4NO(g) +6H2O(g)的平衡常数K=____________________________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的SO2,
①若氨水与SO2恰好完全反应生成正盐,则此时溶液呈_____性(填“酸”或“碱”)常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10ˉ5mol·Lˉ1;H2SO3 :Ka1=1.3×10ˉ2mol·Lˉ1,Ka2=6.3×10ˉ8mol·Lˉ1
②上述溶液中通入______气体可使溶液呈中性,(填“SO2”或NH3”)此时溶液离子浓度由大到小的顺序_________________________________。
【答案】 △H=―1260kJ·molˉ1 A I ![]() E 碱 SO2 c(NH4+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
E 碱 SO2 c(NH4+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
【解析】(1)4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H=反应物的键能总和-生成物的键能总和
2N2(g) +6H2O(g) △H=反应物的键能总和-生成物的键能总和
=![]() =―1260kJ·molˉ1 。
=―1260kJ·molˉ1 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,A.使用催化剂时,可降低该反应的活化能,加快其反应速率,A正确;B.若测得容器内4v正(NH3)=6v逆(H2O)时,两速率之比不等于化学计量数之比,说明反应未达平衡,B不正确;C.当容器内![]() =1时,并不能说明各组分含量保持不变,也不能说明正、逆反应速率相等,所以不能说明反应已达平衡,C不正确。
=1时,并不能说明各组分含量保持不变,也不能说明正、逆反应速率相等,所以不能说明反应已达平衡,C不正确。
(3)①根据图像结合N元素守恒可知,在高温时氨主要转化为NO,所以该催化剂在高温时选择反应I。
② 520℃时,4NH3(g)+5O2![]() 4NO(g) +6H2O(g)的平衡常数可根据A点数据计算.A点对应的纵坐标为0.2,说明n(N2)=n(NO)=0.2mol,根据N元素守恒得n(NH3)=1-0.2-0.2
4NO(g) +6H2O(g)的平衡常数可根据A点数据计算.A点对应的纵坐标为0.2,说明n(N2)=n(NO)=0.2mol,根据N元素守恒得n(NH3)=1-0.2-0.2![]() =0.4mol,再根据H元素守恒得n(H2O)=
=0.4mol,再根据H元素守恒得n(H2O)= ![]() ,最后根据O元素守恒得n(O2)=2-
,最后根据O元素守恒得n(O2)=2- ![]() -
- ![]() = 1.45mol,所以K=
= 1.45mol,所以K= ![]() 。
。
③使用催化剂Pt/Ru可以加快化学反应速率,但不能提高反应物的转化率,所以A和B都不正确; C.增大NH3和O2的初始投料比会减小氨气的转化率,C不正确; D.正反应是气体分子数变多的方向,投料比不变,增加反应物的浓度相当于采取了加压的措施,加压对逆反应有利,所以氨的转化率减小,D不正确; E.正反应是放热反应,所以降低反应温度对正反应有利,有利于提高NH3转化为N2平衡转化率,所以E正确。
(4)①若氨水与SO2恰好完全反应生成正盐即亚硫酸铵,溶液中铵根和亚硫酸根都会水解,铵根水解使溶液呈酸性,而亚硫酸根水解则使溶液呈碱性,由于Ka2=6.3×10ˉ8mol·Lˉ1小于Kb=1.8×10ˉ5mol·Lˉ1,根据越弱越水解,溶液的酸碱性由水解程度更大的离子决定,所以此时溶液呈碱性。由于亚硫酸氢根的电离程度大于其水解程度,亚硫酸氢铵溶液呈酸性(由Kb和Ka1=1.3×10ˉ2mol·Lˉ1的相对大小也能得出这个结论)
②由①的分析可知上述溶液中通入SO2气体可使溶液呈中性,即常温下溶液pH=7,由Ka2=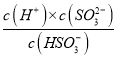 =6.3
=6.3![]() ,把c(H+)=1
,把c(H+)=1![]() 代入,得
代入,得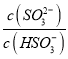 =6.3
=6.3![]() ,所以c(HSO3-)>c(SO32-)。此时溶液中的溶质为(NH4)2SO3和NH4HSO3的混合物,因为盐类水解的程度一般是很小的,所以溶液中离子浓度由大到小的顺序:c(NH4+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)。
,所以c(HSO3-)>c(SO32-)。此时溶液中的溶质为(NH4)2SO3和NH4HSO3的混合物,因为盐类水解的程度一般是很小的,所以溶液中离子浓度由大到小的顺序:c(NH4+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)。

 精英口算卡系列答案
精英口算卡系列答案【题目】草酸晶体的组成可表示为H2C2O4·xH2O,某研究性学习小组用下图装置进行“草酸晶体受热分解的部分产物的验证”的实验。请回答下列问题。

【资料查阅】
①草酸晶体在101 ℃时开始熔化,150 ℃时开始升华,175 ℃时开始分解;
②草酸钙和草酸氢钙均为白色不溶物。
(1)按照如图所示的装置,通过实验检验草酸晶体的部分分解产物,装置B中可观察到有气泡冒出且澄清石灰水变浑浊,由此甲同学判断草酸晶体分解的产物中有CO2。但立即遭到乙同学反对,其反对的理由可能是______________________________________。
(2)丙同学认为草酸晶体分解的产物中含有CO,为进行验证,X应选用________(填化学式)浓溶液,装置D的作用是____________________。
(3)实验过程中涉及如下操作:①点燃装置A处的酒精灯;②熄灭装置A处的酒精灯;③点燃装置E处的酒精灯;④熄灭装置E处的酒精灯。这4步操作由先到后的顺序为____________(填序号)。点燃E处酒精灯前必须要进行的操作是______________。
(4)实验过程中发现装置E中黑色粉末变红色,装置F中有黑色固体生成,经检测装置F中的固体为金属单质,则装置F中发生反应的化学方程式为________________________________________________________________________。
(5)丁同学用滴定法测定草酸晶体中结晶水的含量,进行了下列操作:
步骤一:用分析天平称取3.15 g纯净的该草酸晶体,配制成250 mL溶液。
步骤二:用移液管移取25.00 mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化。
步骤三:取0.100 mol·L-1标准酸性KMnO4溶液,进行滴定,三次结果如下表所示:
第一次 | 第二次 | 第三次 | |
待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知滴定反应的离子方程式为:MnO![]() +H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
+H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
①配制草酸溶液的操作步骤依次是:将晶体置于烧杯中,加水溶解,将溶液转移入________,洗涤,定容,摇匀。
②通过计算确定x=________。