��Ŀ����
���ڹ�����ռ����Ҫ��λ��
��1����ҵ�ϳɰ�ʱ���ϳ�����ÿ����1 mol NH3���ų�46.1 kJ��������
�� ��ҵ�ϳɰ����Ȼ�ѧ����ʽ�� ��
�� ��֪��
N2 (g)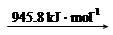 2N (g)
2N (g)
H2 (g)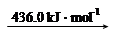 2H (g)
2H (g)
��Ͽ�1 mol N��H�������������_______kJ��
��2���±��ǵ���Ӧ���а�n(N2):n(H2)=1:3Ͷ�Ϻ���200�桢400�桢600���£���Ӧ�ﵽƽ��ʱ���������NH3�����ʵ���������ѹǿ�ı仯���ߡ�
�� ����a��Ӧ���¶��� ��
�� ���ڹ�ҵ�ϳɰ��ķ�Ӧ������������ȷ���� ������ĸ����
A. ��ʱ�����NH3�������H2��ƽ��ת����
B. �Ӵ����ܼӿ췴Ӧ���������H2��ƽ��ת����
C. ��ͼ��M��N��Q��ƽ�ⳣ��K�Ĵ�С��ϵ��K(M)=" K(Q)" >K(N)
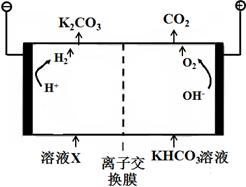
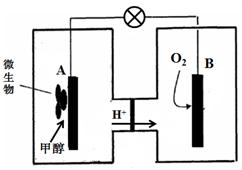
�� M���Ӧ��H2ת������ �� ��3������һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϡ���ص��ܷ�ӦΪ��
��3������һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϡ���ص��ܷ�ӦΪ��
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)��
���ȼ�ϵ�صĸ�����Ӧʽ�� ��
��1����N2(g)+ 3H2(g)  2NH3(g)����H =" ��92.2" kJ��mol-1�� 391��2���� 200�棻�� AC���� 75%��3��2NH3��6e�� + 6OH��= N2 + 6H2O
2NH3(g)����H =" ��92.2" kJ��mol-1�� 391��2���� 200�棻�� AC���� 75%��3��2NH3��6e�� + 6OH��= N2 + 6H2O
���������������1���ٺϳ�����ÿ����1mol NH3���ų�46.1kJ�����������Ȼ�ѧ����ʽд������ע���ʾۼ�״̬�Ͷ�Ӧ��Ӧ�ų����������Ȼ�ѧ����ʽ��N2��g��+3H2��g�� 2NH3��g������H=-92.2kJ/mol���ڷ�Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�������=3��436+945.8-6��N-H������=-92.2��N-H������=391kJ��2���ϳɰ���ӦΪ���ȷ�Ӧ����Ӧ�¶�Խ��Խ�����ڷ�Ӧ�Ľ��У�����a��NH3�����ʵ���������ߣ��䷴Ӧ�¶�Ӧ�����ͣ���aΪ200���A����ʱ�����NH3����ʹƽ�������ƶ�����A��ȷ��B�������ܼӿ췴Ӧ���ʣ������ܸı�ת���ʣ���B����Cƽ�ⳣ��K���¶��йأ������������أ�ͬһ�¶��µ�ƽ�ⳣ����ȣ��ϳɰ���ӦΪ���ȷ�Ӧ�����¶�Խ��ƽ�ⳣ��ԽС����C��ȷ��ѡAC������M��NH3�����ʵ���Ϊ60%��ʣ�����ʵ���Ϊ40%����n(N2):n(H2)=1:3Ͷ�ϣ���ʣ��H2���ʵ���Ϊ30%����ΪN2��g��+3H2��g��
2NH3��g������H=-92.2kJ/mol���ڷ�Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�������=3��436+945.8-6��N-H������=-92.2��N-H������=391kJ��2���ϳɰ���ӦΪ���ȷ�Ӧ����Ӧ�¶�Խ��Խ�����ڷ�Ӧ�Ľ��У�����a��NH3�����ʵ���������ߣ��䷴Ӧ�¶�Ӧ�����ͣ���aΪ200���A����ʱ�����NH3����ʹƽ�������ƶ�����A��ȷ��B�������ܼӿ췴Ӧ���ʣ������ܸı�ת���ʣ���B����Cƽ�ⳣ��K���¶��йأ������������أ�ͬһ�¶��µ�ƽ�ⳣ����ȣ��ϳɰ���ӦΪ���ȷ�Ӧ�����¶�Խ��ƽ�ⳣ��ԽС����C��ȷ��ѡAC������M��NH3�����ʵ���Ϊ60%��ʣ�����ʵ���Ϊ40%����n(N2):n(H2)=1:3Ͷ�ϣ���ʣ��H2���ʵ���Ϊ30%����ΪN2��g��+3H2��g�� 2NH3��g������������Ӧ��H2���ʵ���Ϊ90%����M���Ӧ��H2ת������
2NH3��g������������Ӧ��H2���ʵ���Ϊ90%����M���Ӧ��H2ת������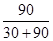 %=75%����3��ԭ����и���ʧȥ���ӣ����ϼ����ߣ�����������Ӧ����Ӧʽ2NH3��6e��+6OH��=N2+6H2O��
%=75%����3��ԭ����и���ʧȥ���ӣ����ϼ����ߣ�����������Ӧ����Ӧʽ2NH3��6e��+6OH��=N2+6H2O��
���㣺�Ȼ�ѧ����ʽ����ѧ�������ܵ��ת������ѧƽ�ⳣ�����㣻��ѧ��Դ���͵�أ�

��ѧ��Ҫ�о���̼Ԫ�ؼ��仯������صĺܶ���⡣
��1����̿��������ȡˮú�������12g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131. 6kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��_________ ��
��2����ҵ�Ͽ��ý�̿ұ����������0.5mol̼��ȫ�������Ӧ���õ�0.6mol����ͬʱ����2�ֳ������壬��÷�Ӧ�Ļ�ѧ����ʽ��_________��
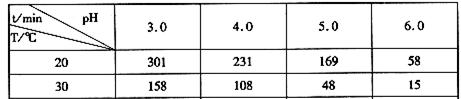
��3��̼��ˮ������ˮú���ķ�Ӧ��һ�����淴Ӧ��������������жϸ÷�Ӧһ���ﵽƽ��״̬����_________��ѡ���ţ�����
| A��V��(H2O)=V��(H2) |
| B���������¶Ȳ��ٷ����ı� |
| C������nmolH2ͬʱ����nmolCO |
| D������������������ʵ�������ʱ��ı� |
 CO(g)+H2(g)��ƽ�ⳣ������ֵΪ_________���ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬������ͼ�л�����5���ӵ�9���Ӻ�c(H2O)Ũ�ȱ仯���Ƶ����ߣ�ֻҪ���Ա�ʾ����
CO(g)+H2(g)��ƽ�ⳣ������ֵΪ_________���ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬������ͼ�л�����5���ӵ�9���Ӻ�c(H2O)Ũ�ȱ仯���Ƶ����ߣ�ֻҪ���Ա�ʾ����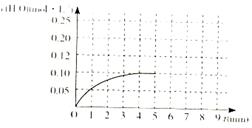
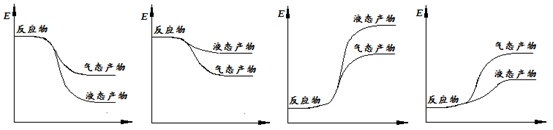
��1�� 8gҺ̬��CH3OH����������ȫȼ�գ����ɶ�����̼�����Һ̬ˮʱ�ͷų�Q kJ����������д��Һ̬CH3OHȼ���ȵ��Ȼ�ѧ����ʽ ��
��2���ڻ�ѧ��Ӧ�����У��ƻ��ɻ�ѧ����Ҫ�����������γ��»�ѧ���ֻ��ͷ�������
| ��ѧ�� | H��H | N��H | N��N |
| ����/kJ·mol��1 | 436 | 391 | 945 |
�Ը��ݱ������м������ݼ���a����ֵΪ�� ��
��3����֪��C(s��ʯī)��O2(g)=CO2(g) ��H1����393.5 kJ/mol
2H2(g)��O2(g)=2H2O(l) ��H2����571.6 kJ/mol
2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l) ��H3����2599 kJ/mol
���ݸ�˹���ɣ���C(s��ʯī)��H2(g)����1 mol C2H2(g)��Ӧ���Ȼ�ѧ����ʽ��
��

 SO3��g����NO��g��
SO3��g����NO��g��