��Ŀ����
����Ŀ�����仯�����������й㷺��;�������λ��ͬ���壬���������ƵĻ�ѧ���ʡ�
(1)���������Ӧ���� BCl3���ڸ÷����У���ԭ���������__________�����ӡ�
(2)��������������Һ��Ӧ���� Na[B(OH)4]�����ǻ��������ƣ����������÷�Ӧ�Ļ�ѧ����ʽΪ____________��
(3)B(OH)3(����)��һԪ���ᣬ����ˮ�����ư��ĵ��룺 NH3+H2O![]() +OH- ��������ˮ�е���ķ���ʽΪ____��
+OH- ��������ˮ�е���ķ���ʽΪ____��
(4)NaBH4 ���л��ϳ�����Ҫ�Ļ�ԭ������ҵ�Ϻϳɷ���֮һ�ǣ�Na2B4O7 +16Na+8H2 +7SiO2 ![]() 7Na2SiO3 +4NaBH4 ���ڸ÷�Ӧ�У���������___________���Ʊ�1 mol NaBH4ʱת�� ____________mol ���ӡ�
7Na2SiO3 +4NaBH4 ���ڸ÷�Ӧ�У���������___________���Ʊ�1 mol NaBH4ʱת�� ____________mol ���ӡ�
(5)NaBH4��ˮ��Ӧ����Na[B(OH)4]��һ�����壬д����ѧ����ʽ��_____________��
���𰸡�6 2B��2NaOH��6H2O��2Na[B(OH)4]��3H2�� H3BO3+H2O [B(OH)4]-+H+ H2 4 NaBH4+4H2O��Na[B(OH)4]+4H2��
��������
(1) Bԭ���������3�����ӣ���������Ӧ���� ��BCl3�������γ�3��B-Cl�������ݴ˷����жϣ�
(2) ��������������Һ��Ӧ���� Na[B(OH)4]���������ݴ���д��Ӧ�Ļ�ѧ����ʽ��
(3)����[B(OH)3]��һԪ���ᣬ����ˮ�����ư��ĵ��룺 NH3+H2O![]() +OH- ����������εĻ�ѧʽΪNa[B(OH)4]��д������ˮ�еĵ��뷽��ʽ��
+OH- ����������εĻ�ѧʽΪNa[B(OH)4]��д������ˮ�еĵ��뷽��ʽ��
(4) ��ӦNa2B4O7 +16Na+8H2 +7SiO2![]() 7Na2SiO3 +4NaBH4��Na�Ļ��ϼ���0�����ߵ�+1�ۣ�HԪ�صĻ��ϼ���0�۽���Ϊ-1�ۣ����������ԭ��Ӧ�Ĺ��ɷ������
7Na2SiO3 +4NaBH4��Na�Ļ��ϼ���0�����ߵ�+1�ۣ�HԪ�صĻ��ϼ���0�۽���Ϊ-1�ۣ����������ԭ��Ӧ�Ĺ��ɷ������
(5)NaBH4��HΪ-1�ۡ�BΪ+3�ۣ�-1�۵�����ˮ��+1���ⷢ��������ԭ��Ӧ����H2��ͬʱ����Na[B(OH)4]���ݴ���д��Ӧ�Ļ�ѧ����ʽ��
(1)Bԭ���������3�����ӣ���������Ӧ���� BCl3���÷������γ�3��B-Cl��������ԭ���������6�����ӣ��ʴ�Ϊ��6��
(2)B��Al�����ʾ��������ԣ���������������Һ��Ӧ���� Na[B(OH)4]����������Ӧ�Ļ�ѧ����ʽΪ2B��2NaOH��6H2O��2Na[B(OH)4]��3H2�����ʴ�Ϊ��2B��2NaOH��6H2O��2Na[B(OH)4]��3H2����
(3)����[B(OH)3]��һԪ���ᣬ����ˮ�����ư��ĵ��룺 NH3+H2O![]() +OH- �������εĻ�ѧʽΪNa[B(OH)4]����������ˮ�еĵ��뷽��ʽ�ǣ�H3BO3+H2O [B(OH)4]-+H+���ʴ�Ϊ��H3BO3+H2O [B(OH)4]-+H+��
+OH- �������εĻ�ѧʽΪNa[B(OH)4]����������ˮ�еĵ��뷽��ʽ�ǣ�H3BO3+H2O [B(OH)4]-+H+���ʴ�Ϊ��H3BO3+H2O [B(OH)4]-+H+��
(4) Na2B4O7 +16Na+8H2 +7SiO2![]() 7Na2SiO3 +4NaBH4����Ӧ��Na�Ļ��ϼ���0�����ߵ�+1�ۣ�HԪ�صĻ��ϼ���0�۽���Ϊ-1�ۣ����������Ϊ��������ԭ��Ϊ�ƣ���Ӧ��ת��16�����ӣ����Ʊ�1 mol NaBH4ʱת��4mol ���ӣ��ʴ�Ϊ��H2��4��
7Na2SiO3 +4NaBH4����Ӧ��Na�Ļ��ϼ���0�����ߵ�+1�ۣ�HԪ�صĻ��ϼ���0�۽���Ϊ-1�ۣ����������Ϊ��������ԭ��Ϊ�ƣ���Ӧ��ת��16�����ӣ����Ʊ�1 mol NaBH4ʱת��4mol ���ӣ��ʴ�Ϊ��H2��4��
(5)NaBH4��HΪ-1�ۡ�BΪ+3�ۣ�-1�۵�����ˮ��+1���ⷢ��������ԭ��Ӧ����H2���൱��ˮ���������������NaBH4��-1�۵�H��ͬʱ����Na[B(OH)4]����Ӧ�Ļ�ѧ����ʽΪ��NaBH4+4H2O��Na[B(OH)4]+4H2�����ʴ�Ϊ��NaBH4+4H2O��Na[B(OH)4]+4H2����

����Ŀ��ijѧ����0.1000 mol/L NaOH��Һ�ζ�δ֪Ũ�ȵ�������Һ�������ɷֽ�Ϊ���¼�����
A.������ˮϴ�ɾ��ζ��ܣ�B. �ô��ⶨ����Һ��ϴ��ʽ�ζ��ܣ�C.����ʽ�ζ���ȡϡ����20.00 mL��ע����ƿ�У������̪��D.��ȡ��ƿ�����ظ�����һ�Σ�E.���ζ����Ƿ�©ˮ��F.ȡ�¼�ʽ�ζ����ñ���NaOH��Һ��ϴ����Һע���ʽ�ζ��ܡ�0���̶�����2��3 cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ������0���̶Ȼ�0���̶����£�
G.����ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶ȡ����������գ�
��1����ȷ������˳����(�������ĸ��д)_____________��
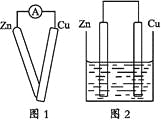
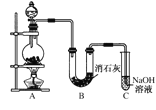
��2������F��Ӧ��ѡ��ͼ��________�ζ���(����)��

��3���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲�________��
A. �ζ�����Һ��ı仯 B. ��ƿ����Һ��ɫ�ı仯
�ζ��յ���Һ��ɫ�ı仯��____________________________��
��4���ζ���������ʾ��
�ζ����� | ������Һ���/mL | ����Һ�����/mL | |
�ζ�ǰ�̶� | �ζ���̶� | ||
1 | 20 | 1.02 | 21.03 |
2 | 20 | 2.00 | 25.00 |
3 | 20 | 0.60 | 20.60 |
�ζ������ϴ���ǵ�________��ʵ�飬����������Ŀ���ԭ����________��
A. ��ʽ�ζ�����װҺǰδ�ñ�NaOH��Һ��ϴ2��3��
B. �ζ���ʼǰ��ʽ�ζ��ܼ��첿�������ݣ��ڵζ��յ����ʱδ��������
C. �ζ���ʼǰ��ʽ�ζ��ܼ��첿��û�����ݣ��ڵζ��յ����ʱ���ּ��첿��������
D. �ﵽ�ζ��յ�ʱ��������Һ��Һ����͵����
E. �ζ������У���ƿҡ����̫���ң�������ЩҺ�ηɽ�����
��5���������Ũ��Ϊ________mol/L��
��6�����ȷ��ȡ20.00 mL 0.1000 mol/L NaOH��Һ����ƿ�У������ָ̪ʾ����Ȼ����δ֪Ũ�ȵ�����(װ����ʽ�ζ�����)�ζ����Ƿ�Ҳ�ɲⶨ����������ʵ���Ũ�ȣ�________(��ǡ���)��