题目内容
16.下列有机化合物转化关系如图所示:
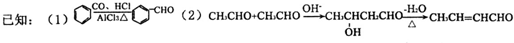
其中化合物A苯环上的一氯代物只有两种.
请回答下列问题:
(1)写出B的结构简式
 .
.(2)①的反应类型为加成反应;化合物F的核磁共振氢谱显示有4个峰.
(3)写出C与新制Cu(OH)2反应的化学方程式
 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O.(4)已知两分子H能形成六元环酯,反应④的化学方程式n
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O.
+nH2O.(5)化合物C有多种同分异构体,请写出满足①遇氯化铁溶液显紫色;②苯环上有三个取代基;③苯环上的一氯取代物只有两种,三种条件的所有同分异构体的结构简式
 或
或 .
.
分析 据已知信息和化合物A苯环上的一氯代物只有两种可知A为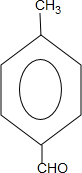 ,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为
,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为 ,B发生消去反应生成C,C为
,B发生消去反应生成C,C为 ,C与新制氢氧化铜反应,醛基被氧化为羧基,D为
,C与新制氢氧化铜反应,醛基被氧化为羧基,D为 ,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为
,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为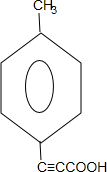 ,两分子H能形成六元环酯,说明H为
,两分子H能形成六元环酯,说明H为 ,D→G是
,D→G是 与HX的加成反应,再在NaOH的水溶液中水解再酸化生成H,据此分析.
与HX的加成反应,再在NaOH的水溶液中水解再酸化生成H,据此分析.
解答 解:(1)据已知信息和化合物A苯环上的一氯代物只有两种可知A为 ,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为
,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为 ,故答案为:
,故答案为: ;
;
(2)D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为 ,F中有4中氢原子,所以核磁共振氢谱显示有4个峰,故答案为:加成反应;4;
,F中有4中氢原子,所以核磁共振氢谱显示有4个峰,故答案为:加成反应;4;
(3)C为 ,C与新制氢氧化铜反应,醛基被氧化为羧基,D为
,C与新制氢氧化铜反应,醛基被氧化为羧基,D为 ,化学方程式为:
,化学方程式为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(4)两分子H能形成六元环酯,说明H为 ,D→G是
,D→G是 与HX的加成反应,再在NaOH的水溶液中加热水解生成H,H通过缩聚反应生成高聚物I的方程式为n
与HX的加成反应,再在NaOH的水溶液中加热水解生成H,H通过缩聚反应生成高聚物I的方程式为n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O,
+nH2O,
故答案为:NaOH的水溶液加热;n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O;
+nH2O;
(5)C为 ,其同分异构体①遇氯化铁溶液显紫色,说明有酚羟基,②苯环上有三个取代基 ③苯环上的一氯取代物只有两种,说明有两个取代基相同,符合条件的有
,其同分异构体①遇氯化铁溶液显紫色,说明有酚羟基,②苯环上有三个取代基 ③苯环上的一氯取代物只有两种,说明有两个取代基相同,符合条件的有 或
或 ,故答案为:
,故答案为: 或
或 .
.
点评 本题考查有机物推断、有机反应类型、官能团判断、有机方程式书写等,难度不大,涉及炔、烯烃的性质与转化,注意对基础知识的理解掌握.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 氢氧化钠溶液 | B. | 水 | C. | 亚硫酸 | D. | 硫酸铜 |
| A. | 检查装置的气密性--制取气体、验证气体的性质等与气体有关的实验操作 | |
| B. | 检查是否漏水--滴定管、容量瓶、分液漏斗等的使用 | |
| C. | 验纯--点燃可燃性气体 | |
| D. | 湿润--用石蕊试纸、碘化钾淀粉试纸和pH 试纸检验或验证某些气体 |
| A. | 加入铝粉放出H2的溶液中:Al3+、K+、SO42-、Cl- | |
| B. | 1.0mol•L-1的KNO3溶液中:Na+、Fe2+、Cl-、SO42- | |
| C. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、HCO3- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液中:K+、Cu2+、SO42-、NO3- |
| A. | 液氯、干冰均为纯净物 | |
| B. | NO2、CO、CO2均为酸性氧化物 | |
| C. |  与 与 互为同系物 互为同系物 | |
| D. | 淀粉、纤维素和油脂都属于天然高分子化合物 |
 把锌片和铁片放在盛有含酚酞的稀食盐水的玻璃器皿中,如图.经过一段时间后,首先观察到溶液变红的区域是( )
把锌片和铁片放在盛有含酚酞的稀食盐水的玻璃器皿中,如图.经过一段时间后,首先观察到溶液变红的区域是( )| A. | Ⅰ和Ⅲ附近 | B. | Ⅰ和Ⅳ附近 | C. | Ⅱ和Ⅲ附近 | D. | Ⅱ和Ⅳ附近 |
| A. | 25℃时,pH=11 NaOH溶液和pH=3 CH3COOH混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | 取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 | |
| C. | 含等物质的量的NaHC2O4和Na2C2O4的溶液中存在:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| D. | 25℃时,某溶液中由水电离出的c(H+)=10-amol/L,若a>7时,该溶液pH一定为14-a |
 、NO
、NO
 、NO
、NO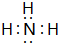 .
.