题目内容
【题目】偏钒酸铵(NH4VO3)主要用作催化剂、催干剂、媒染剂等。用沉淀法除去工业级偏钒酸铵中的杂质硅、磷的流程如图:
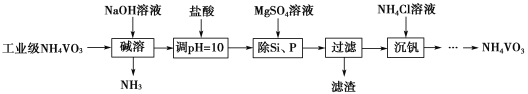
(1)碱溶时,下列措施有利于NH3逸出的是____(填字母序号)。
a.升高温度 b.增大压强 c.增大NaOH溶液的浓度
(2)①滤渣的主要成分为Mg3(PO4)2、MgSiO3,已知Ksp(MgSiO3)=2.4×10-5,若滤液中c(SiO32-)=0.08mol·L-1,则c(Mg2+)=____。
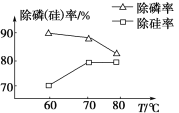
②由图可知,加入一定量的MgSO4溶液作沉淀剂时,随着温度的升高,除磷率下降,其原因是温度升高,Mg3(PO4)2溶解度增大和促进Mg2+水解生成Mg(OH)2;但随着温度的升高,除硅率升高,其原因是____(用离子方程式表示)。
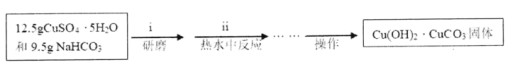
(3)沉钒时,反应温度需控制在50℃,在实验室可采取的加热方式为____。
(4)探究NH4Cl的浓度对沉钒率的影响,设计实验步骤(常见试剂任选):取两份10mL一定浓度的滤液A和B,分别加入1mL和10mL的1mol·L-1 NH4Cl溶液,再向A中加入___mL蒸馏水,控制两份溶液的温度均为50℃、pH均为8,由专用仪器测定沉钒率,加入蒸馏水的目的是____。
(5)偏钒酸铵本身在水中的溶解度不大,但在草酸(H2C2O4)溶液中因发生氧化还原反应而溶解,同时生成络合物(NH4)2[(VO)2(C2O4)3],该反应的化学方程式为____。
【答案】ac 3×10-4mol·L-1 ![]() (或
(或![]() ) 水浴加热 9 使两份溶液总体积相等,确保其他条件相同,而NH4Cl的浓度不同 2NH4VO3+4H2C2O4=(NH4)2[(VO)2(C2O4)3]+2CO2↑+4H2O
) 水浴加热 9 使两份溶液总体积相等,确保其他条件相同,而NH4Cl的浓度不同 2NH4VO3+4H2C2O4=(NH4)2[(VO)2(C2O4)3]+2CO2↑+4H2O
【解析】
工业级钒酸铵先用NaOH溶液溶解,生成NaVO3,再加入盐酸调节溶液的PH=10后加入MgSO4溶液,使Si、P转化为Mg3(PO4)2、MgSiO3沉淀而除去,过滤后滤液中加入NH4Cl溶液,生成NH4VO3。
(1)气体溶解度随温度升高而降低,所以加热可以使NH3逸出。在溶有NH3的溶液中,存在平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,增大OH-浓度,可以使平衡逆移,也促使NH3逸出;故选ac;
NH4++OH-,增大OH-浓度,可以使平衡逆移,也促使NH3逸出;故选ac;
(2)①滤液中c(SiO32-)=0.08mol·L-1,根据Ksp(MgSiO3)=2.4×10-5,则c(Mg2+)=![]() mol/L;
mol/L;
②温度升高,硅酸根离子水解程度增大,可以成为H2SiO3沉淀从而提高除硅率,离子方程式为![]() (或
(或![]() );
);
(3)温度在100℃以下,可以用水浴加热法,水浴加热不但可以受热均匀,而且温度易于控制,故答案为:水浴加热;
(4)要探究NH4Cl的浓度对沉钒率的影响,一份10mL的滤液A中加入1mL NH4Cl溶液,另一份10mL的滤液B中加入10mL NH4Cl溶液,需再向A中加入9mL蒸馏水,使两份溶液总体积相等,确保其他条件相同,而NH4Cl的浓度不同。故答案为:9,使两份溶液总体积相等,确保其他条件相同,而NH4Cl的浓度不同;
(5)偏钒酸铵和草酸(H2C2O4)发生氧化还原反应,生成络合物(NH4)2[(VO)2(C2O4)3],矾的化合价从+5价降低到+4价,那么碳的化合价就会从+3价升高到+4价,根据电子守恒,得到该反应的化学方程式为2NH4VO3+4H2C2O4=(NH4)2[(VO)2(C2O4)3]+2CO2↑+4H2O。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】A和B两种有机物可以互溶,有关性质如下:
物质 | 密度(g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
A | 0.7893 | -117.3 | 78.5 | 与水以任意比混溶 |
B | 0.7137 | -116.6 | 34.5 | 不溶于水 |
(1)要除去A和B的混合物中的少量B,可采用的_______________方法可得到A。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
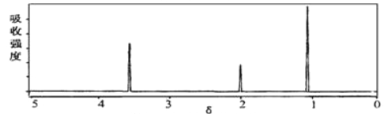
(2)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应且消耗6.72L(标准状况)氧气,生成5.4gH2O和8.8gCO2,则该物质的实验式是__________;质谱图显示,A的相对分子质量为46,又已知有机物A的核磁共振氢谱如图所示,则A的结构简式为________________。
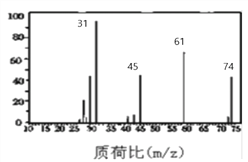
(3)下图是B的质谱图,则其相对分子质量为 ________ ,
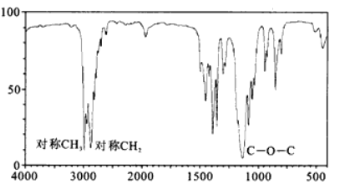
(4)B的红外光谱如图所示,则B的结构简式为__________________________。
(5)准确称取一定质量的A和B的混合物,在足量氧气充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增加14.4g和26.4g。计算混合物中A和B的物质的量之比_____________________。