题目内容
【题目】Ⅰ.①![]() H与
H与![]() H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷![]() ;④甲烷(CH4)与丙烷(C3H8)。
;④甲烷(CH4)与丙烷(C3H8)。
(1)互为同位素的是______ (填序号,下同)。
(2)互为同系物的是______。
(3)互为同分异构体的是______。
(4)互为同素异形体的是______。
II.A~E等几种烃分子的球棍模型如下图所示,据此回答下列问题。
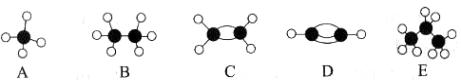
(1)D的电子式为___________,A的二氯取代物有 种。
(2)可作为植物生长调节剂的是 (填结构简式);
(3)A与氯气反应可以生成多种物质,试任写其中一个反应的化学方程式: ;
(4)C与水在一定条件下反应的化学方程式为: 。
【答案】Ⅰ(1)①;(2)④;(3)③;(4)②;II. (1)![]() ,1;(2)CH2=CH2;(3)CH4 +Cl2
,1;(2)CH2=CH2;(3)CH4 +Cl2![]() CH3Cl +HCl、 CH3Cl +Cl2
CH3Cl +HCl、 CH3Cl +Cl2![]() CH2Cl2 +HCl、CH2Cl2 +Cl2
CH2Cl2 +HCl、CH2Cl2 +Cl2![]() CHCl3 +HCl、CHCl3 +Cl2
CHCl3 +HCl、CHCl3 +Cl2![]() CCl4 +HCl;(4)CH2=CH2+H2O
CCl4 +HCl;(4)CH2=CH2+H2O![]() CH3CH2OH。
CH3CH2OH。
【解析】
试题分析:I.(1)同位素:具有相同的质子数,不同中子数的同种元素不同核素,即①;同系物:组成和结构相似,组成相差一个或若干个“CH2”的化合物,即④;(3)同分异构体:分子式相同,结构不同的化合物,即③;(4)同素异形体:同种元素组成不同结构的单质,即②;II.(1)D为C2H2,其电子式为:![]() ,A为甲烷,空间结构为正四面体,因此二氯代物只有1种;(2)可作植物生长调节剂的是C2H4;(3)甲烷和氯气发生取代反应是连锁反应,其反应方程式为:CH4 +Cl2
,A为甲烷,空间结构为正四面体,因此二氯代物只有1种;(2)可作植物生长调节剂的是C2H4;(3)甲烷和氯气发生取代反应是连锁反应,其反应方程式为:CH4 +Cl2![]() CH3Cl +HCl、 CH3Cl +Cl2
CH3Cl +HCl、 CH3Cl +Cl2![]() CH2Cl2 +HCl、CH2Cl2 +Cl2
CH2Cl2 +HCl、CH2Cl2 +Cl2![]() CHCl3 +HCl、CHCl3 +Cl2
CHCl3 +HCl、CHCl3 +Cl2![]() CCl4 +HCl;(4)C为乙烯,和水在一定条件下发生加成反应,CH2=CH2+H2O
CCl4 +HCl;(4)C为乙烯,和水在一定条件下发生加成反应,CH2=CH2+H2O![]() CH3CH2OH。
CH3CH2OH。

 阅读快车系列答案
阅读快车系列答案【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________。

(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为______________微粒之间存在的作用力是_____________。
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为______。
,0)。则D原子的坐标参数为______。
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为__________g·cm-3(列出计算式即可)。