题目内容
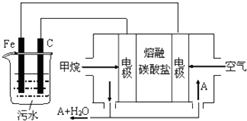
20.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣.此时,应向污水中加入适量的c.
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ.Fe-2e-=Fe2+
Ⅱ.4OH--4e-=2H2O+O2↑;
(3)以上电解过程是图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极.
①正极的电极反应是O2+2CO2+4e-=2CO32-;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环.A物质的化学式是CO2;
(4)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)11.2L.
分析 (1)能使导电能力增强的电解质必须是易溶于水的,且只能是中性的;
(2)根据阳极电极材料和离子的放电顺序考虑放电的离子,并书写电极反应式;
(3)①燃料电池中,正极发生的反应一定是氧气得电子的过程;
②电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳;
(4)在燃料电池和电解池的串联电路中,转移的电子数目是相同的.
解答 解:(1)保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀时,加入的使导电能力增强的电解质必须是可溶于水的、显中性的盐,故答案为:c;
(2)电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,同时也发生副反应,即溶液中的OH-失电子被氧化生成O2,故答案为:2H2O-4e-=4H++O2↑;
(3)①料电池中,正极反应一定是氧气的电子的过程,该电池的电解质环境是熔融碳酸盐,所以电极反应为:O2+2CO2+4e-=2CO32- (或2O2+4CO2+8e-=4CO32-),故答案为:O2+2CO2+4e-=2CO32- (或2O2+4CO2+8e-=4CO32-);
②电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳,故答案为:CO2;
(4)阴极的电极反应为:2H++2e-=H2↑,阴极产生了44.8L(标准状况)即2mol的氢气产生,所以转移电子的物质的量为4mol,根据电池的负极电极反应是CH4+4CO32--8e-=5CO2+2H2O,当转移4mol电子时,消耗CH4(标准状况)的体积V=nVm=0.5mol×22.4L/mol=11.2L,故答案为:11.2L.
点评 本题考查了燃料电池的工作原理和原电池和电解池串联的综合知识,难度较大.

练习册系列答案
相关题目
10.下列有关物质检验的操作和实验结论都正确的是( )
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 向溶液中加NaOH溶液并加热,将干燥红色石蕊试纸放在试管口,试纸变蓝. | 该溶液中一定含NH4+ |
| A. | A | B. | B | C. | C | D. | D |
11.下列有机化合物的名称错误的是( )
| A. | 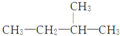 2-甲基丁烷 2-甲基丁烷 | B. |  3-乙基戊烷 3-乙基戊烷 | C. |  2-乙基戊烷 2-乙基戊烷 | D. |  2,3-二甲基丁烷 2,3-二甲基丁烷 |
8.下列对化学反应的认识正确的是( )
| A. | 化学反应过程中,分子的种类和数目一定发生改变 | |
| B. | 对一可逆反应,其他条件不变时,升高温度,平衡常数K一定增大 | |
| C. | 化学反应过程中,一定有化学键的断裂和形成 | |
| D. | 放热反应的反应速率,一定比吸热反应的反应速率大 |
15.下列说法正确的是( )
| A. | 干冰升华和液氯气化时要破坏不同的微粒间作用力 | |
| B. | CO2和SiO2具有相同的化学键类型和晶体类型 | |
| C. | 水结成冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| D. | 盐酸能电离出氢离子和氯离子,所以HCl中存在离子键 |
5.钠与水反应时的现象可以概括为“熔成小球、浮在水面、四处游走、嘶嘶作响、加入酚酞变红”,下列钠的性质中与反应现象无关的是( )
| A. | 钠的熔点低 | B. | 钠的硬度小 | ||
| C. | 钠的密度小 | D. | 钠的化学性质活泼 |
12.Na、Mg、O、Cl四种元素中只能以离子键结合的化合物有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
10.下列有机物中,属于烷烃的是( )
| A. | C2H6 | B. | C2H2 | C. | C6H6 | D. | C2H4O |