题目内容
8.能说明氧的非金属性比硫强的是( )①氢硫酸溶液在空气中置露会变浑浊
②在通常状况下,氧单质的熔沸点比硫单质低
③硫化氢在加热的条件下既可分解成氢气和硫,而水在高温时很少分解
④铜与硫反应生成硫化亚铜,与氧气反应生成氧化铜.
| A. | ①③④ | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
分析 比较非金属元素的非金属性强弱,可根据单质之间的置换反应、对应最高价氧化物的水化物的酸性、氢化物的稳定性等角度判断.
解答 解:①氢硫酸溶液在空气中置露会变浑浊,说明氧气的氧化性大于硫,由元素的非金属性越强对应单质的氧化性越强,可知氧的非金属性比硫强,故正确;
②单质的熔沸点与非金属性无关,在通常状况下,氧单质的熔沸点比硫单质低,不能说明氧的非金属性比硫强,故错误;
③元素的非金属性越强,对应氢化物的稳定性越强,硫化氢在加热的条件下既可分解成氢气和硫,而水在高温时很少分解,则水比硫化氢稳定,则氧的非金属性比硫强,故正确;
④铜与硫反应生成硫化亚铜,与氧气反应生成氧化铜,说明氧气的氧化性大于硫,则氧的非金属性比硫强,故正确;
故选A.
点评 本题考查非金属性的判断,题目难度不大,注意非金属性的递变规律以及比较非金属性的角度.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
19.在一定条件下RO3-与R-发生如下反应:RO3-+5R-+6H+=3R2+3H2O,则下列关于R元素的说法中正确的是( )
| A. | R位于元素周期表中的第VA族 | B. | R位于元素周期表中的第 VIIA族 | ||
| C. | RO3-中的R元素只能被还原 | D. | R2在常温常压下一定是气体 |
3.下列说法错误的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 在共价化合物中一定含有共价键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 全部由非金属组成的化合物可能是离子化合物 |
13.将充满NO2 和O2混合气体的量筒倒立于水中,充分反应后,保持气体的压强不变,水进入至量筒容积的一半处停止了,则原混合气体中NO2 和O2的体积比( )
| A. | 3:2 | B. | 2:3 | C. | 11:9 | D. | 1:3 |
16.用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是( )
| A. | 配制标准溶液的NaOH中混有Na2CO3杂质 | |
| B. | 滴定终点读数时,俯视滴定管的刻度,其他操作正确 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗 | |
| D. | 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
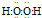 .
.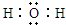 ,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑
,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑ 向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)请回答下列问题:
向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)请回答下列问题: