题目内容
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验。
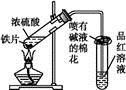
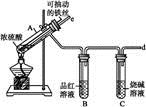
图1 图2
(1)比较两实验装置,图2装置的优点是:
①能更好地吸收有毒气体SO2,防止其污染环境;
② 。(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而污染环境;二是 。(3)能说明有SO2气体产生的实验现象是 。(4)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
E.NaOH溶液 F.淀粉KI溶液
G.H2O2溶液


图1 图2
(1)比较两实验装置,图2装置的优点是:
①能更好地吸收有毒气体SO2,防止其污染环境;
② 。(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而污染环境;二是 。(3)能说明有SO2气体产生的实验现象是 。(4)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
| A.稀HCl溶液 | B.稀H2SO4溶液 |
| C.KSCN溶液 | D.KMnO4溶液 |
G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的 (填试剂序号,下同),振荡,再滴加少量的 ,根据溶液颜色的变化可确定假设Ⅱ是否正确。反应的离子方程式是 ,Fe3++3SCN- Fe(SCN)3。验证III:步骤1.取试样,滴加少量的 (填试剂序号),溶液的颜色变 色,则试样中含有Fe3+。步骤2.再取适量的试样滴加到少量的 (填试剂序号),观察到的现象为 ,则试样中含有Fe2+。(1)便于控制反应的进行
Fe(SCN)3。验证III:步骤1.取试样,滴加少量的 (填试剂序号),溶液的颜色变 色,则试样中含有Fe3+。步骤2.再取适量的试样滴加到少量的 (填试剂序号),观察到的现象为 ,则试样中含有Fe2+。(1)便于控制反应的进行
(2)停止加热时,防止倒吸或平衡压强(凡答案合理均可)
(3)品红溶液褪色
(4)验证Ⅱ: C G H2O2+2Fe2++2H+ 2Fe3++2H2O
2Fe3++2H2O
验证III:C(或F) 红(或蓝)
D 紫色褪去或变浅
 Fe(SCN)3。验证III:步骤1.取试样,滴加少量的 (填试剂序号),溶液的颜色变 色,则试样中含有Fe3+。步骤2.再取适量的试样滴加到少量的 (填试剂序号),观察到的现象为 ,则试样中含有Fe2+。(1)便于控制反应的进行
Fe(SCN)3。验证III:步骤1.取试样,滴加少量的 (填试剂序号),溶液的颜色变 色,则试样中含有Fe3+。步骤2.再取适量的试样滴加到少量的 (填试剂序号),观察到的现象为 ,则试样中含有Fe2+。(1)便于控制反应的进行(2)停止加热时,防止倒吸或平衡压强(凡答案合理均可)
(3)品红溶液褪色
(4)验证Ⅱ: C G H2O2+2Fe2++2H+
 2Fe3++2H2O
2Fe3++2H2O验证III:C(或F) 红(或蓝)
D 紫色褪去或变浅
(1)图2装置除多了一个吸收装置外,还有一根可抽动的铁丝,抓住不同点进行分析即可;(4)验证Ⅱ首先加入KCSN溶液,验证溶液中无Fe3+,然后再加入氧化剂把Fe2+氧化为Fe3+,进行鉴别,因为KMnO4溶液有颜色,所以不能作为此反应的氧化剂;验证III首先加入KCSN溶液验证溶液中有Fe3+,然后再验证溶液中的Fe2+,因为原溶液中有Fe3+,所以不能用把Fe2+氧化为Fe3+,滴加KCSN溶液进行鉴别的方法,所以只能用KMnO4溶液鉴别。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


 H2SO3
H2SO3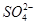
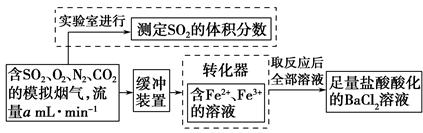
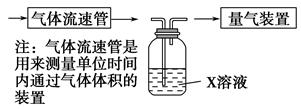
 的转化率,已知气体流速,还需测定的数据有 、 。
的转化率,已知气体流速,还需测定的数据有 、 。
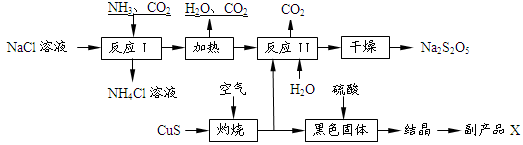
 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。