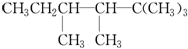题目内容
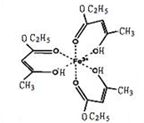 氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.
氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.(1)此配合物中,铁离子的价电子排布式为
(2)此配合物中碳原子的杂化轨道类型有
考点:配合物的成键情况,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)铁元素是26号元素,铁原子核外有26个电子,铁原子失去3个电子变成铁离子,根据构造原理写出其价电子排布式;
(2)根据碳原子含有的σ键和孤电子对个数确定杂化类型,碳原子的杂化轨道和氢原子的1s轨道形成化学键;
(2)根据碳原子含有的σ键和孤电子对个数确定杂化类型,碳原子的杂化轨道和氢原子的1s轨道形成化学键;
解答:
解:(1)铁元素是26号元素,其原子核外有26个电子,铁原子失去3个电子变成铁离子,其价电子排布式为:3d5,故答案为:3d5;
(2)甲基和乙基上的碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,碳碳双键两端的碳原子含有3个σ键且不含孤电子对,所以采取杂化sp2,-C2H5中C-H间碳原子的sp3杂化轨道和氢原子的1s轨道形成化学键,
故答案为:sp3、sp2,碳原子的sp3杂化轨道和氢原子的1s轨道;
(2)甲基和乙基上的碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,碳碳双键两端的碳原子含有3个σ键且不含孤电子对,所以采取杂化sp2,-C2H5中C-H间碳原子的sp3杂化轨道和氢原子的1s轨道形成化学键,
故答案为:sp3、sp2,碳原子的sp3杂化轨道和氢原子的1s轨道;
点评:本题主要考查了核外价电子的排布、原子杂化轨道、及化学键的形成等知识,难度不大,解题时要注意基础知识的应用.

练习册系列答案
相关题目
向体积和物质的量浓度均相等的盐酸与NaOH溶液中,分别加入足量的铝粉,充分反应后盐酸中产生氢气V1 mL,NaOH溶液中产生氢气V2 mL(体积均在相同条件下测定),下列说法中正确的是( )
①V1=V2
②二者转移电子的物质的量之比为1:3
③反应后的两溶液相混合,铝元素将全部沉淀
④铝与NaOH溶液反应时,H2O作氧化剂.
①V1=V2
②二者转移电子的物质的量之比为1:3
③反应后的两溶液相混合,铝元素将全部沉淀
④铝与NaOH溶液反应时,H2O作氧化剂.
| A、②③ | B、①②③ |
| C、②③④ | D、全部 |
下列化学实验现象描述不正确的是( )
| A、氯气使湿润的红纸条褪色 |
| B、石蕊试液滴入稀硫酸溶液中显红色 |
| C、淀粉溶液遇碘酒变蓝色 |
| D、往硫酸铜溶液中滴加氢氧化钠溶液出现红褐色沉淀 |