��Ŀ����
����Ŀ���״���һ����;�dz��㷺�Ļ�������ԭ�ϣ���ͨ�����з�Ӧ�ϳɣ�
��CO��g��+2H2��g�� ![]() CH3OH��g����H1
CH3OH��g����H1
��CO2��g��+3H2��g�� ![]() CH3OH��g��+H2O��g����H2
CH3OH��g��+H2O��g����H2
��CO��g��+H2O��g�� ![]() CO2��g��+H2��g����H3
CO2��g��+H2��g����H3
�ش���������
��1����Ӧ������S________������>������<����0����H1=________������H2����H3��ʾ����
��2��������Ӧ��ƽ�ⳣ������Ȼ����ֵlnKP��KPΪ�Է�ѹ��ʾ��ƽ�ⳣ�������¶ȵĹ�ϵ��ͼ����ʾ
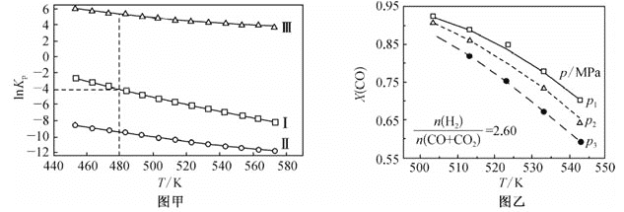
�ٷ�Ӧ������H________������>������<����0��
��480Kʱ��lnKP����+lnKp����+lnKp����=________��
��ij�¶��£���ij�����ܱ������г���0.1 molCO��0.2molH2������Ӧ�����ﵽƽ��ʱ��CO��ת����Ϊ90%����ƽ��ʱ��ѹǿ5MPa����KP=________��KPΪ�Է�ѹ��ʾ��ƽ�ⳣ������ѹ=��ѹ�����ʵ�����������
��3������CO��CO2�������ϳɼ״�����ʼʱ������ ![]() =2.60��CO��ƽ��ת����X��CO�����¶ȼ�ѹǿ�Ĺ�ϵ��ͼ����ʾ������˵����ȷ����_____������ĸ����
=2.60��CO��ƽ��ת����X��CO�����¶ȼ�ѹǿ�Ĺ�ϵ��ͼ����ʾ������˵����ȷ����_____������ĸ����
A p1<p2<p3
B �����¶ȣ���Ӧ���ʺ�X��CO������С
C ��ʼʱ��p2=7.2MPa����H2�ķ�ѹΪ5.2MPa
D �����������䣬���� ![]() ��X��CO������
��X��CO������
���𰸡�< ��H2+��H3 < -8 12.96 CD
��������
(1)���ݷ�Ӧǰ������������仯ȷ����S�����ݸ�˹���ɼ��㷴Ӧ����H1��
(2)�ٸ����¶ȶ�K��Ӱ�������Ӧ����ЧӦ��
�ڸ���ͼ�����¶�Ϊ480Kʱ����Ӧ��lnKpֵ���м��㼴�ɣ�
�۸���ƽ������ʽ�����Kp�ı���ʽ���м��㣻
(3)A.���ѹǿ��ƽ���ƶ���Ӱ�������
B.����¶ȶԷ�Ӧ���ʺ�ƽ���ƶ���Ӱ�������
C.����ѹǿ֮�ȵ������ʵ���֮�Ƚ��м��㣻
D.����Ũ�ȶ�ƽ���ƶ���Ӱ�������
(1)��Ӧ��Ӧ�������������С������S<0����֪����CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)��H2����CO(g)+H2O(g)
CH3OH(g)+H2O(g)��H2����CO(g)+H2O(g)![]() CO2(g)+H2(g)��H3�����ݸ�˹���ɣ��ɢ�+��ɵ�CO(g)+2H2(g)
CO2(g)+H2(g)��H3�����ݸ�˹���ɣ��ɢ�+��ɵ�CO(g)+2H2(g)![]() CH3OH(g)����Ӧ���Ƿ�Ӧ����H1= ��H2+��H3��
CH3OH(g)����Ӧ���Ƿ�Ӧ����H1= ��H2+��H3��
(2)����ͼ��֪�����¶�����ʱ��lnKp��С����Kp��С��˵�������¶ȣ�ƽ�������ƶ����淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ�������H<0��
�����ڷ�Ӧ�����ͨ����Ӧ��͢���ӵõ�������Kp(��)= Kp(��) Kp(��)������lnKp(��)= Kp(��) +Kp(��)=-4����ͼ��֪�����¶�Ϊ480Kʱ��lnKp(��)=-4������lnKp(��)+lnKp(��)+lnKp(��)=-4-4=-8��
��ƽ��ʱCO��ת����Ϊ90%������뷴Ӧ��n(CO)=0.1mol��90%=0.09mol�����ݷ�Ӧ�Ļ�ѧ����ʽ��֪�����뷴Ӧ��n(H2)=0.09mol��2=0.18mol����Ӧ���ɵ�n(CH3OH)=0.09mol����Ӧ�ﵽƽ��ʱn(CO)=0.1mol-0.09mol=0.01mol��n(H2)=0.2mol-0.18mol=0.02mol��n(CH3OH)=0.09mol����ƽ��ʱCO�����ķ�ѹ![]() ��H2�����ķ�ѹ
��H2�����ķ�ѹ![]() ��CH3OH�����ķ�ѹ
��CH3OH�����ķ�ѹ![]() ����˸÷�Ӧ�÷�ѹ��ʾ��ƽ�ⳣ��
����˸÷�Ӧ�÷�ѹ��ʾ��ƽ�ⳣ��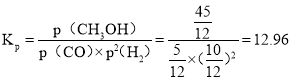 ��
��
(3)A.���ںϳɼ״��ķ�ӦΪ�����������С�ķ�Ӧ���������ѹǿ��ƽ�������ƶ���CO��ת�������������ͬ�¶��£� ת����Խ��ѹǿԽ��p1>p2>p3����A����
B.�����¶ȣ���Ӧ���ʼӿ죬��B����
C.����![]() �� ��˿���n(H2)=2.60mol��n(CO+CO2)=1.00mol������ѹǿ֮�ȵ������ʵ���֮�ȣ��ɵõ�ʽ
�� ��˿���n(H2)=2.60mol��n(CO+CO2)=1.00mol������ѹǿ֮�ȵ������ʵ���֮�ȣ��ɵõ�ʽ![]() �� ��
�� ��![]() �� ���p(H2)=0.52MPa����C��ȷ��
�� ���p(H2)=0.52MPa����C��ȷ��
D.������������ʱ������![]() �� ���൱������c(H2)��ƽ�������ƶ���CO��ƽ��ת��������D��ȷ��
�� ���൱������c(H2)��ƽ�������ƶ���CO��ƽ��ת��������D��ȷ��
�ʴ�Ϊ��CD��

����Ŀ������ȩ��һ����Ҫ�Ļ���ԭ�ϣ�ijС��ͬѧ������ͼ��ʾʵ��װ��(�г�װ������ȥ)�Ʊ�����ȩ����֪�л��������������±���ʾ��
�л��� | �е��� | �ܶ�Ϊg/cm3 | ��Է��� ���� | �ܽ��� |
����ȩ | 178.1 | 1.045 | 106 | ����ˮ���������Ҵ����Ѻ�±���� |
���״� | 205.7 | 1.045 | 108 | ����ˮ���������Ҵ����Ѻ�±���� |
���ȼ��� | 39.8 | 1.33 | ������ˮ���������л��ܼ� |

ʵ�鲽�裺
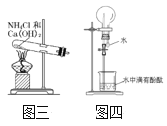
�����ݻ�Ϊ500mL��������ƿ����90.0mL��������Ϊ5%�Ĵ���������Һ(�Թ���)��������Һ��pHΪ9��10����3.1mL(Լ3.24g)���״���75.0mL���ȼ��飬���Ͻ��衣
����ַ�Ӧ���ö��ȼ�����ȡˮ��3�Σ������л���ϲ���
���������л����м�����ˮ����þ�����ˣ��õ��л�����
�������л������õ�1.908g����ȩ��Ʒ��
��ش��������⣺
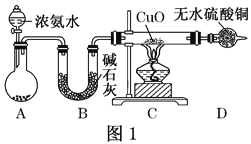
��1������b������Ϊ______����������������______��
��2�����״���NaClO��Ӧ�Ļ�ѧ����ʽΪ_______��
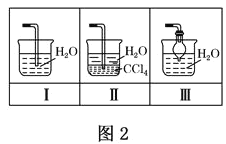
��3���������У�Ͷ��ʱ���������Ʋ��ܹ���̫�࣬ԭ����____���������м�����ˮ����þ����ʡ�Ըò����� ������ɵĺ����______��
��4���������У�Ӧѡ�õ�ʵ��װ����___(�����)��


��5���������У������¶�Ӧ������_______���ҡ�
��6����ʵ���У�����ȩ�IJ���Ϊ________(������С�����һλ)��
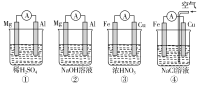
����Ŀ�������й�ʵ�����������ͽ��۶���ȷ���ǣ� ��
ѡ�� | ʵ����� | ���� | ���� |
A | ϡ������Һ�м���������۳�ַ�Ӧ�μ�KSCN��Һ | ��Һ��ΪѪ��ɫ | ϡ������������ԣ��ܽ�Fe������Fe3+ |
B | ��AgNO3��Һ�еμӹ�����ˮ | ��Һ���� | Ag+��NH3��H2O�ܴ������� |
C | ��ij��Һ�еμ�ϡNaOH��Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿ� | ��ֽ���� | ����Һ�д���NH4+ |
D | ���з�̪��Na2CO3��Һ�м���������BaCl2���� | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
A. AB. BC. CD. D
����Ŀ��ij�¶��£���2L�����ܱ������г���1molA��1molB��������ӦA(g)+B(g) ![]() C(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ��� ��
C(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ��� ��
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.��Ӧ��ǰ5s��ƽ������V(A)=0.03mol/(L��s)
B.���������������䣬�����¶ȣ�ƽ��ʱc(A)=0.41mol��L-1����Ӧ����H>0
C.��ͬ�¶��£���ʼʱ�������г���2.0molC���ﵽƽ��ʱ��C�ķֽ��ʴ���80%
D.��ͬ�¶��£���ʼʱ�������г���0.2molA.0.2molB��1.0molC����Ӧ�ﵽƽ��ǰ��Ӧ����V������<V���棩