题目内容
6.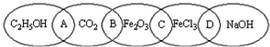 如图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号,请回答下列问题:
如图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号,请回答下列问题:(1)两种物质都是非电解质的是A(填分类标准代号,下同),两种物质在水溶液中都能导电的是D.
(2)分类标准代号C表示B.
A.两物质一定不与同一种酸反应 B.两物质都是电解质
C.两物质都是铁盐 D.两物质可以通过一步反应相互转化
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,此反应的离子方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(4)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,得到的分散系称为胶体,相应的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
分析 (1)根据非电解质的定义及电解质溶液导电的原因分析;
(2)根据分类标准C是Fe2O3和FeCl3所共有的性质来分析;
(3)根据题意分析得出两种物质间的关系,从而确定该物质,并写出相应的方程式.
(4)根据请氧化铁胶体的制作方法分析并写出反应方程式.
解答 解:(1)在水溶液里或熔融状态下都不导电的化合物是非电解质,乙醇和二氧化碳都是非电解质,故选A;
含有自由移动的离子的水溶液就能导电,易溶性的电解质溶液就能导电,故选D.
故答案为:A;D;
(2)分类标准C是Fe2O3和FeCl3所共有的性质.
A.两物质可以与同一种酸,如HI反应,故A错误;
B.Fe2O3在熔融状态下能导电,FeCl3在水溶液中和熔融状态下均能导电,故两物质都是电解质,故B正确;
C.Fe2O3是氧化物,不是铁盐,故C错误;
D.Fe2O3和盐酸反应能一步生成FeCl3,但FeCl3需要至少两步才能反应生成Fe2O3,故D错误.
故选B;
(3)某一物质能与某种强酸反应生成上述中的另一种物质,所以这两种物质应有相同的元素,且化合价不变,所以是氧化铁和氯化铁,
化学反应方程式为:Fe2O3+6HCl=2FeCl3+3H2O,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
(4)该方法是制作氢氧化铁胶体,反应方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl
故答案为:胶体;FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
点评 本题考查了电解质、非电解质的区分、物质的分类方法等知识点,要注意:胶体区别于其它分散系的本质特征是胶体粒子直径介于1-100nm之间,而不是丁达尔效应,丁达尔效应是物理变化不是化学变化.

 优加精卷系列答案
优加精卷系列答案| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=2,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=0.2 | |
| B. | 参加反应的氯气的物质的量等于0.5a mol | |
| C. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$a mol≤ne≤$\frac{5}{6}$a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{a}{6}$mol |
| A. | 加电解质可使某种胶体聚沉,这是中和胶体粒子所带电荷的缘故 | |
| B. | 胶体粒子在直流电场中做定向移动,这是胶体粒子选择性吸附离子而带电荷的缘故 | |
| C. | 一束光线通过胶体时有丁达尔效应,这是胶体粒子对光散射的缘故 | |
| D. | 由于胶体粒子带电荷,所以胶体这种分散系不是电中性的 |
| A. | 在 101kPa 下,1克物质燃烧所放出的热量叫做该物质的热值 | |
| B. | 金属的防腐处理中,牺牲阳极的阴极保护法是电解池原理的应用 | |
| C. | 活化分子间的碰撞就是有效碰撞 | |
| D. | 催化剂能增大单位体积内活化分子百分数,从而增大反应速率 |
| A. | 常温常压下,48gO2跟48gO3 含有的氧原子数均为3NA | |
| B. | 1L 0.5mol/L的(NH4)2SO4溶液中含有NH4+数目为NA | |
| C. | 标准状况下,11.2L 氨气所含有的原子数是4NA | |
| D. | 80gNaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L |