题目内容
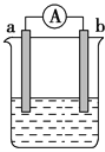
【题目】全钒氧化还原液流电池是一种新型绿色的二次电池。其工作原理如图所示。下列叙述正确的是

A.电子由Y极流出,经质子交换膜到X极
B.放电过程中,电解质溶液pH降低
C.Y极反应式为V2+-e-=V3+
D.每转移1 mol,电子理论上有2 mol H+由交换膜右侧向左侧迁移
【答案】C
【解析】
电池是高考常考题型之一,主要涉及电极判断、电极反应式的书写、离子移动、PH变化、计算。
A. 观察装置,由物质转化可以确定右边发生氧化反应,Y极为负极,左边发生还原反应,X为正极。电子只能在导线上迁移,即电子由Y极经导线流向X极,故A错误。
B. 放电过程中,电池反应式为V2++VO2++2H+=V3++VO2++H2O,消耗H+,pH升高,故B错误。
C. Y极为负极,发生氧化反应,由离子转化关系知反应式为V2+-e-=V3+,故C正确。
D. X极反应式为VO2++2H++e-=VO2++H2O,得失电子数决定氢离子迁移数目。转移1mol电子,只有1molH+迁移,故D错误。
故答案选C。

练习册系列答案
相关题目
【题目】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a | |||||||||||||||||
b | c | d | e | ||||||||||||||
f | g | ||||||||||||||||
h | |||||||||||||||||
(1)请画出上述元素h的原子结构示意图_______;元素h位于元素周期表的第_____区。
(2)e、g两种元素的气态氢化物中更稳定的是_______(写化学式);
(3)b2a2分子的电子式是________ ,该分子中存在的σ键与π键的个数比为_______。
(4)c、d两种元素中第一电离能较大的是_________(写元素符号)。
(5)f和g两种元素形成的化合物是______(填“离子化合物”“共价化合物”)。a2d分子是_________分子(填极性分子或者非极性分子)。