题目内容
【题目】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。
2SO3(g)。
(1)降低温度,化学反应速率___(填“增大”“减小”或“不变”)。
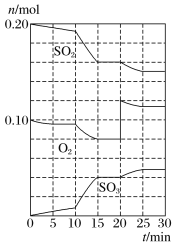
(2)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,反应前15min用SO3表示的平均反应速率为___。
(3)已知0-15min反应放出的总热量为QkJ,写出该反应的热化学方程式____。
(4)根据如图判断,10min时改变的反应条件可能是___(填编号,下同);20min时改变的反应条件可能是____。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质的量
【答案】减小 1.33×10-3mol·L-1·min-1 2SO2(g)+O2(g)![]() 2SO3(g) △H=-50QkJ/mol ab d
2SO3(g) △H=-50QkJ/mol ab d
【解析】
(1)结合温度对速率的影响分析;
(2)根据n=![]() 计算前15min内用SO2表示的平均反应速率;
计算前15min内用SO2表示的平均反应速率;
(3)根据反应方程式中的计量进行计算,求出2 mol SO3时放出的总热量,从而得到热化学方程式;
(4)10min到15min的时间段,化学反应速率加快,二氧化硫和氧气的量减小,三氧化硫的量增加;反应进行至20min时,氧气的物质的量增加,二氧化硫的减少,三氧化硫的增加,据此分析。
(1)降低温度,化学反应速率减小;
(2) 15min时三氧化硫的物质的量为0.04mol,前15min内用SO3表示的平均反应速率为:v(SO3)=![]() =1.33×10-3mol/(Lmin);
=1.33×10-3mol/(Lmin);
(3) 15min时SO3的物质的量为0.04mol,此时放出的总热量为QkJ,则生成2 mol SO3时放出的总热量为![]() =50QkJ,该反应的热化学方程式为2SO2(g)+O2(g)
=50QkJ,该反应的热化学方程式为2SO2(g)+O2(g)![]() 2SO3(g) △H=-50QkJ/mol;
2SO3(g) △H=-50QkJ/mol;
(4)根据图象所示信息,10min到15min的时间段,化学反应速率加快,可以是加了催化剂或者是增大压强,或缩小容器体积,故答案为ab;
反应进行至20min时,氧气的物质的量增加,二氧化硫的减少,三氧化硫的增加,可以推断是增加了O2的量,故答案为d。

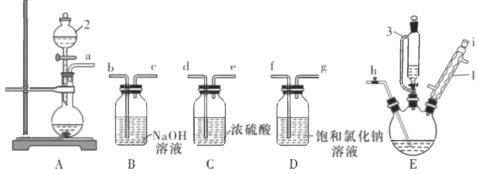
【题目】某小组拟设计实验探究乙醇的还原性及产物,装置如图所示。
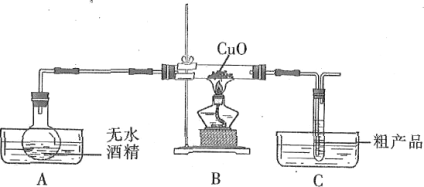
已知:几种有机物的部分物理性质如表所示:
有机物 | 乙醇 | 乙酸 | 乙醛 |
溶解性 | 易溶于水和乙酸、乙醛 | 易溶于水和乙醇、乙醛 | 易溶于水和乙醇、乙酸 |
沸点 | 78.5 | 117.9 | 20.8 |
(1)为了获得比较稳定的气流,A装置还缺少一种仪器是____(填仪器名称)。A装置使用____(填“冷水浴”或“热水浴”)。
(2)当B中氧化铜完全反应后,正确的操作排序为____(填序号)。
①从C装置中取出试管 ②继续通入乙醇蒸气至B装置中的试管冷却
③熄灭酒精灯 ④从A装置中取出烧瓶
(3)分离和提纯产品。实验完毕后,取少量粗产品于试管,滴加紫色石蕊溶液,溶液变红色,则粗产品中含有___(填化学式)。对粗产品进行____操作(填名称)可以获得较纯的乙醛。
(4)已知:Cu2O呈红色,在酸性条件下发生反应为Cu2O+2H+=Cu+Cu2++H2O。乙同学取少量B中红色粉末于试管,滴加稀硫酸溶液,观察到____(填实验现象),证明红色产物中含有Cu2O。