题目内容
【题目】有物质的量浓度均为![]() 的①
的①![]() 溶液 ②
溶液 ②![]() 溶液③
溶液③ ![]() 溶液各25mL,下列说法正确的是
溶液各25mL,下列说法正确的是
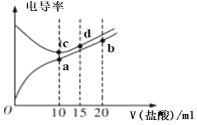
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是①
C.若分别加入25mL ![]() 盐酸后,pH最小的是②
盐酸后,pH最小的是②
D.若升高温度,则③的pH不变
【答案】C
【解析】
A. 等浓度时强碱的pH最大,强碱弱酸盐中对应的酸性越强,水解程度越小,碳酸氢根离子的酸性小于醋酸,所以3种溶液pH的大小顺序是![]() ,故A错误;
,故A错误;
B. 稀释时强碱的变化程度大,所以三种溶液稀释相同倍数,pH变化最大的是![]() ,故B错误;
,故B错误;
C. 等体积等浓度混合后,![]() 中溶质为
中溶质为![]() 、NaCl,
、NaCl,![]() 中溶质为NaCl、
中溶质为NaCl、![]() ,
,![]() 中溶质为NaCl,而
中溶质为NaCl,而![]() 离子水解显碱性,所以pH最大的是
离子水解显碱性,所以pH最大的是![]() ,pH最小的是
,pH最小的是![]() ,故C正确;
,故C正确;
D. 若升高温度,水的离子积常数变大,则![]() 的pH变小,故D错误。
的pH变小,故D错误。
综上所述,答案为C。

【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L
【题目】I、下图为汽车尾气处理系统中“三元催化”的工作原理,NO和CO在催化剂作用下生成无污染性物质的方程式2NO+2CO![]() N2+2CO2。
N2+2CO2。
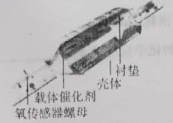
某课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
实验编号 | 实验目的 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 同种催化剂的比表面积/m2·g-1 | c(CO)不变时所用的时间/min |
① | 参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
② | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
③ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
(1)实验编号②的实验目的为_______。
(2)课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是________。
II、某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
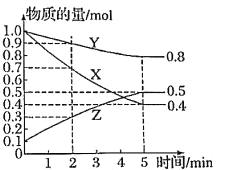
(1)该反应的化学方程式是______。
(2)该反应达到平衡状态的标志是
A. Y的体积分数在混合气体中保持不变
B. X、Y的反应速率比为3:1
C. 容器内气体压强保持不变
D. 容器内气体的总质量保持不变
E. 生成1 mol Y的同时消耗2 mol Z
(3)2~5min内用X表示的化学反应速率为_____。