题目内容
【题目】I、下图为汽车尾气处理系统中“三元催化”的工作原理,NO和CO在催化剂作用下生成无污染性物质的方程式2NO+2CO![]() N2+2CO2。
N2+2CO2。
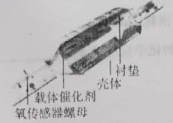
某课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
实验编号 | 实验目的 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 同种催化剂的比表面积/m2·g-1 | c(CO)不变时所用的时间/min |
① | 参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
② | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
③ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
(1)实验编号②的实验目的为_______。
(2)课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是________。
II、某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
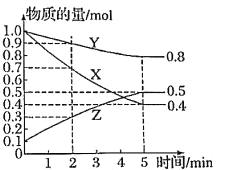
(1)该反应的化学方程式是______。
(2)该反应达到平衡状态的标志是
A. Y的体积分数在混合气体中保持不变
B. X、Y的反应速率比为3:1
C. 容器内气体压强保持不变
D. 容器内气体的总质量保持不变
E. 生成1 mol Y的同时消耗2 mol Z
(3)2~5min内用X表示的化学反应速率为_____。
【答案】探究同种催化剂的比表面积对反应速率的影响 温度 3X(g)+Y(g)2Z(g) AC 0.025mol·L-1·min-1
【解析】
I、根据控制变量的实验探究思想进行分析解答;
II、(1)根据参加反应的各物质的物质的量的变化量之比等于其化学计量数之比判断该反应的化学方程式;
(2)根据化学平衡状态的判断标准进行分析;
(3)根据化学反应速率的计算公式进行计算。
I、(1)实验①和实验②的反应条件中,除了同种催化剂的比表面积大小不同以外,其它条件完全相同,说明实验编号②的实验目的是探究同种催化剂的比表面积对反应速率的影响;
(2)实验①和实验③的反应条件中,除了温度不同以外,其它条件完全相同,可见是探究温度对速率的影响;
II、(1)根据图知,随着反应的进行,X、Y的物质的量逐渐减少,Z的物质的量逐渐增加,则X和Y是反应物,Z是生成物,反应达到平衡时,△n(X)=(1.0-0.4)mol=0.6mol、△n(Y)=(1.0-0.8)mol=0.2mol、△n(Z)=(0.5-0.1)mol=0.4mol,同一可逆反应中同一段时间内参加反应的各物质的物质的量的变化量之比等于其化学计量数之比,X、Y、Z的计量数之比=0.6mol:0.2mol:0.4mol=3:1:2,则该反应的化学方程式为3X(g)+Y(g)2Z(g);
(2)A. Y的体积分数在混合气体中保持不变,说明各物质的量不变,反应达到平衡状态,故A正确;
B. X、Y的反应速率比为3:1时,如果反应速率都是指同一方向的反应速率,则该反应不一定达到平衡状态,故B错误;
C. 该反应前后气体物质的量发生变化,随着反应进行,容器内压强减小,当容器内气体压强保持不变时,各物质的物质的量不变,反应达到平衡状态,故C正确;
D. 各物质均为气态,反应前后容器内气体的总质量一直保持不变,不能判定反应是否达到平衡状态,故D错误;
E. 无论反应是否达到平衡状态都存在生成1molY同时消耗2molZ,速率同向,不能据此判断平衡状态,故E错误;
故选AC;
(3)2~5min内,△n(X)=(0.7-0.4)mol=0.3mol,则用X表示的化学反应速率为![]() 。
。

【题目】完成下列填空:
(1)下图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,写出N2和H2反应的热化学方程式:____________________.

(2)若已知下列数据:试根据表中及图中数据计算N-H的键能____________kJ·mol-1.
化学键 | H-H | N≡N |
键能/kJ·mol-1 | 435 | 943 |
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后E1和E2的变化是:E1___________,E2 _________ (填“增大”、“减小、”“不变”)。
(4)用NH3催化还原NOX还可以消除氮氧化物的污染。例如4NH3(g)+3O2(g)=2N2(g)+6H2O(g);ΔH1= a kJ·mol-1N2(g)+O2(g)=2NO(g);ΔH2=b kJ/mol若1mol NH3还原NO至N2,写出该反应的热化学方程式__________(ΔH用a、b表示).