��Ŀ����
����Ŀ����Ҫ��������и�С��
��1��25��Cʱ��0.1 mol��L��1NH4Cl��Һ��pH____7(�����������������)����ԭ����_________(�����ӷ���ʽ��ʾ)��
��2�����������ܵ��������ڵ���ʵ���________(�����)��
A.�� B.���� C.�Ȼ��ƾ��� D.������������
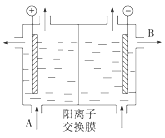
��3�����������ӽ���Ĥ����ⱥ��ʳ��ˮ��NaOH���乤��ԭ������ͼ��ʾ��
����д��A��B�������ʵ����ƣ�A_______________��B__________________��
����д�����ʳ��ˮ�����ӷ���ʽ__________________________________________��
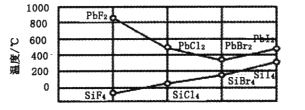
��4���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�� �ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��25��ʱ1Ħ��������ȫת��Ϊ�����ų�92.4KJ��������д����ҵ�ϳɰ����Ȼ�ѧ����ʽ____________��
��5���ϳɰ���ԭ����H2����ͨ����ӦCO(g) + H2O(g)![]() CO2 (g) + H2(g) ��ȡ��
CO2 (g) + H2(g) ��ȡ��
��T ��ʱ�����ݻ��̶�Ϊ5 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08 mol��L-1����ƽ��ʱCO��ת����Ϊ_______�����¶��·�Ӧ��ƽ�ⳣ��KֵΪ_________��
�ڱ����¶���ΪT �棬ֻ�ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ�������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬����_____________������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n(CO) : n(H2O) : n(CO2) : n(H2) �� 1: 16 : 6 : 6
���𰸡��� NH4++H2O![]() NH3��H2O+H+ D ����ʳ��ˮ �������� 2Cl- +2H2O
NH3��H2O+H+ D ����ʳ��ˮ �������� 2Cl- +2H2O ![]() Cl2��+H2��+2OH- N2(g)+3H2(g)=2NH3(g) ��H=-92.4KJ/mol 60% 9/4 cd
Cl2��+H2��+2OH- N2(g)+3H2(g)=2NH3(g) ��H=-92.4KJ/mol 60% 9/4 cd
��������
��1��NH4Cl����ǿ�������Σ�笠�����ˮ����Һ�����ԣ�
��2�����ݵ���ʡ��ǵ���ʵĸ�������жϣ����ʵ���������Ǻ��������ƶ������ӻ����ɵ������ݴ˽��з�����
��3����������������������������������ͼʾװ���еĽ���Ĥ�������ӽ���Ĥ��A������Ҫ�DZ���NaCl��Һ��B������Ҫ������������Һ��װ���ǵ�ⱥ��ʳ��ˮ�����������Ȼ��ƺ�ˮ��Ӧ�����������ƺ������������������Ϸ��������
��4������ͼ����Ϣ��֪���ϳɰ���ӦΪ���ȷ�Ӧ�����25��ʱ1Ħ��������ȫת��Ϊ�����ų�92.4KJ��������д���ϳɰ����Ȼ�ѧ����ʽ��
��5�������ݻ�ѧƽ������ʽ��ʽ����ƽ��Ũ�������ƽ�ⳣ���������õ���
�����ݻ�ѧƽ��״̬,��Ӧ�����淴Ӧ������ͬ,���ɷֺ������ֲ��������
��1��NH4Cl����ǿ����������笠�����ˮ����Һ��������pH��7�����ӷ���ʽΪ��NH4++H2O![]() NH3��H2O+H+��
NH3��H2O+H+��
��������������������� ��NH4++H2O![]() NH3��H2O+H+��
NH3��H2O+H+��
��2��A.���ǵ���,���ǵ����,��A������
B.�����ǻ����,���ǵ����,��B������
C.�Ȼ�����ˮ��Һ�������״̬���ܵ���Ļ�����,�ǵ����,���Dz����������ƶ������ӻ����ɵ���,������,��C������
D.�����������ƺ��������ƶ��������ܹ�����,�ǵ����,��D��ȷ��
��������������ѡD��
��3����������������������������������ͼʾװ���еĽ���Ĥ�������ӽ���Ĥ��A������Ҫ�DZ���NaCl��Һ��B������Ҫ������������Һ��װ���ǵ�ⱥ��ʳ��ˮ�����������Ȼ��ƺ�ˮ��Ӧ�����������ƺ���������������Ӧ�����ӷ���ʽΪ��2Cl- +2H2O ![]() Cl2��+H2��+2OH-��
Cl2��+H2��+2OH-��
��ˣ�������ȷ����������ʳ��ˮ������������2Cl- +2H2O ![]() Cl2��+H2��+2OH-��
Cl2��+H2��+2OH-��
��4������ͼ�������ݿ�֪���¶�������Kֵ��С���÷�Ӧ����ӦΪ���ȷ�Ӧ����25��ʱ1mol������ȫת��Ϊ�����ų�92.4KJ����������÷�Ӧ���Ȼ�ѧ����ʽΪN2(g)+3H2(g)=2NH3(g) ��H=-92.4KJ/mol��
�������������������N2(g)+3H2(g)=2NH3(g) ��H=-92.4KJ/mol��
��5�������ݻ�ѧƽ������ʽ��ʽ����ƽ��Ũ�ȣ�T ��ʱ�����ݻ��̶�Ϊ5L�������г���1molˮ������1molCO����Ӧ��ƽ����CO��Ũ��Ϊ0.08molL-1��
CO��g��+H2O��g���TCO2��g��+H2��g��
��ʼ����mol/L�� 0.2 0.2 0 0
�仯����mol/L�� 0.12 0.12 0.12 0.12
ƽ������mol/L�� 0.08 0.08 0.12 0.12
ƽ��ʱCO��ת����=0.12/0.2=��100%=60%������¶��·�Ӧ��ƽ�ⳣ��K=��0.12��0.12��/��0.08��0.08��=9/4��
��ˣ�������ȷ���ǣ�60%��9/4��
�ڻ�ѧƽ��״̬����Ӧ�����淴Ӧ������ͬ�����ɷֺ������ֲ������ѡ�CO��g��+H2O��g���TCO2��g��+H2��g������Ӧ������������䷴Ӧ��
a����Ӧ�����к�ƽ��״̬��ѹǿ��ͬ��������ѹǿ����ʱ��ı䣬����˵����Ӧ�ﵽƽ��״̬����a�����ϣ�
b��������������غ㣬��Ӧǰ������������䣬��Ӧ�����к�ƽ��״̬�£����������ܶȲ���ʱ��ı䣬����˵����Ӧ�ﵽƽ��״̬����b�����ϣ�
c����λʱ��������amolCO2��ͬʱ����amolH2��˵��������̼�����������淴Ӧ������ͬ��˵����Ӧ�ﵽƽ��״̬����c���ϣ�
d���������n��CO����n��H2O����n��CO2����n��H2��=1��16��6��6�����ݷ�Ӧǰ���������ʵ�����ͬ�������������ʵ�������Ũ�ȼ���Ũ���̺�ƽ�ⳣ���Ƚϣ�Q=6��6/1��16=2.25=K��˵����Ӧ�ﵽƽ��״̬����d���ϣ�
��ˣ�������ȷ���ǣ�cd��

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�