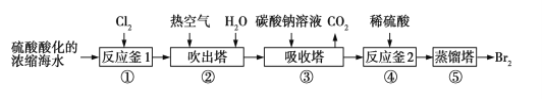
题目内容
【题目】分析化学中常用X射线研究晶体结构,有一种晶体可表示为[MxFey(CN)z],研究表明它的结构特性是Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,其晶体中的阴离子晶胞结构如图所示,下列说法正确的是( )
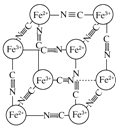
A.该晶体属于原子晶体
B.M的离子位于上述晶胞的面心,呈+2价
C.M的离子位于上述晶胞体心,呈+1价
D.晶体的化学式可表示为MFe2(CN)6,且M为+1价
【答案】D
【解析】
试题分析:A、该结构中存在阴、阳离子,所以一定不是原子晶体,而是离子晶体,A错误;B、Fe2+、Fe3+ 分别占据立方体的顶点,则铁离子与亚铁离子的个数是4×1/8=1/2,而CN一位于立方体的棱上,则CN-的个数是12×1/4=3,所以M、Fe、CN-的个数比是x:2:6,则x+2+3=6,所以x=1,该晶体的化学式是MFe2(CN)6,则M离子为+1价,B错误;C、因为该晶胞中铁离子与亚铁离子的个数是4×1/8=1/2,相当于2个晶胞拥有1个M+,C错误;D、该晶体的化学式是MFe2(CN)6,且M为+1价,D正确,答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目