题目内容
【题目】工业上以浓缩海水为原料提取溴的部分流程如右图:下列说法正确的是
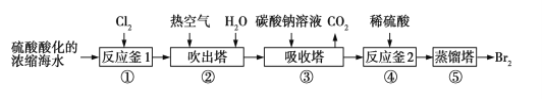
A. 海水需要浓缩,是因为海水中的Br2含量较低
B. 热空气的作用是将多余的Cl2吹出
C. 吸收塔中发生的反应是3Br2+3CO32-=5Br-+BrO3-+3CO2↑
D. 反应釜2中发生的反应是5Br-+BrO3-+3H2O=3Br2+6OH-
【答案】C
【解析】
A. 由于海水中溴离子含量较低,因此海水需要浓缩,海水中不存在单质溴,A错误;
B. 热空气的作用是将生成的溴排入吸收塔中,B错误;
C. 吸收塔中单质溴与碳酸钠反应,反应的方程式为3Br2+3CO32-=5Br-+BrO3-+3CO2↑,C正确;
D. 溶液显酸性,则反应釜2中发生的反应是5Br-+BrO3-+6H+=3Br2+3H2O,D错误。
答案选C。

练习册系列答案
相关题目
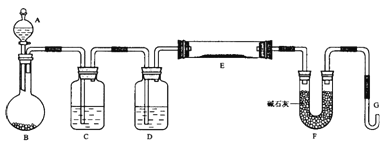
【题目】实验室利用反应TiO2(s)+CCl4(g)=TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4装置如下图所示
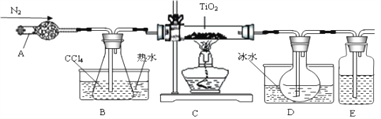
有关物质的性质如下表
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | -23 | 76 | 与TiCl4互溶 |
TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
下列说法正确的是
A. A和E分别盛装碱石灰和氢氧化钠溶液
B. 点燃C处酒精灯后再往A中通入N2
C. TiCl4遇潮湿空气反应的化学方程式:TiCl4+3H2O=H2TiO3+4HCl
D. 分离D中的液态混合物,所采用操作的名称是萃取