��Ŀ����
19��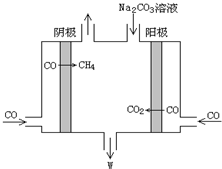 �״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£�
�״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£���CO��g��+2H2��g��?CH3OH��g����H1
��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H2
��CO2��g��+H2��g��?CO��g��+H2O��g����H3
�ش��������⣺
��1����֪��Ӧ���е���صĻ�ѧ�������������£�������CO�е�̼����ΪC$\frac{\underline{\;��\;}}{\;}$O��
| ��ѧ�� | H-H | C-O | C$\frac{\underline{\;��\;}}{\;}$O | H-O | C-H |
| E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | 413 |
��2����25�桢101KPa�£�ÿ���ȼ��1g CH3OH���ָ���ԭ״̬�����ͷ�22.68KJ����������д����ʾ�״�ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-725.76kJ•mol-1��
��3������CO2��H2��Ӧ���ɺϳɶ����ѣ�CH3OCH3������KOHΪ�������Һ����ɶ����ѿ���ȼ�ϵ�أ��õ�ع���ʱ�为����Ӧʽ��CH3OCH3-12e-+16OH-=2CO32-+11H2O��
��4�������£��ö�����ȼ�ϵ�ص��600mL NaCl��Һ�������Ķ�����0.23g����������������1.344L����״��������Һ��pH=13��
��5�����ö�����ȼ�ϵ�ص��CO�Ʊ�CH4��W������ԭ����ͼ��ʾ��������WNaHCO3�ǣ����������ӷ���ʽ��4CO+3CO32-+5H2O=6HCO3-+CH4����
���� ��1����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ����ݸ�˹���ɣ���Ӧ��-��Ӧ��=��Ӧ�ۣ���Ӧ��Ҳ������Ӧ�ļ��㣻
��2������ȼ���ȸ�����1mol��ȼ����ȫȼ�������ȶ�������ų����������������������32g�״�ȼ�����ɶ�����̼��Һ̬ˮ���ȣ�����Ȼ�ѧ����ʽ��д��������ע���ʾۼ�״̬�Ͷ�Ӧ�ʱ䣻
��3������ȼ�ϵ��Ϊȼ��������ʧ���ӷ���������Ӧ����ϵ������Һ��д�����缫��Ӧʽ��
��4������ȼ�ϵ�صĵ缫��Ӧ��֪��������ת�Ƶ�����Ŀ�Ĺ�ϵ�����õ����غ㣬��Ϸ�Ӧ2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+Cl2��+H2�����м��㣻
��5���ɴ˵��ԭ����֪������ʧȥ�������ɶ�����̼���壬����̼���ƣ�̼�����������̼��Ӧ����̼�����ƣ�����CO�õ��������ɼ������壬�ݴ˽�ɣ�
��� �⣺��1����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ��ʡ�H1=1076kJ��mol-1+2��436kJ��mol-1-��3��413+343+465��kJ��mol-1=-99kJ��mol-1��
���ݸ�˹���ɣ���Ӧ��-��Ӧ��=��Ӧ�ۣ��ʡ�H3=��H2-��H1=-58kJ��mol-1-��-99kJ��mol-1��=+41kJ��mol-1��
�ʴ�Ϊ��-99��+41��
��2����25�桢101kPa�£�1g�״���CH3OH��ȼ������CO2��Һ̬ˮʱ����22.68kJ��32g�״�ȼ�����ɶ�����̼��Һ̬ˮ�ų�����Ϊ725.76KJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-725.76kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-725.76kJ•mol-1��
��3��ȼ�ϵ��Ϊȼ��������ʧ���ӷ���������Ӧ���ֵ������ҺΪKOH�����Ը����缫��ӦʽΪ��CH3OCH3-12e-+16OH-=2CO32-+11H2O��
�ʴ�Ϊ��CH3OCH3-12e-+16OH-=2CO32-+11H2O��
��4������ȼ�ϵ�صĵ缫��ӦCH3OCH3-12e-+16OH-�T2CO32-+11H2O��֪����0.23g�����ѿ�ת�Ƶ��ӵ����ʵ���Ϊ$\frac{0.23}{46}��12$mol=0.06mol�����ݷ�Ӧ2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+Cl2��+H2����֪����ת��0.06mol����ʱ������NaOH�����ʵ���Ϊ0.06mol�����������������ʵ�����Ϊ0.03mol�����������������������Ϊ0.03��2��22.4L=1.344L��NaOH�����ʵ���Ũ��Ϊ0.06mol��600mL=0.1mol/L��������Һ��pHֵΪ13��
�ʴ�Ϊ��1.344L��13��
��5���ɴ˵��ԭ����֪������ʧȥ�������ɶ�����̼���壬����̼���ƣ�̼�����������̼��Ӧ����̼�����ƣ�����CO�õ��������ɼ������壬�ݴ����ӷ�Ӧ����ʽΪ��4CO+3CO32-+5H2O=6HCO3-+CH4����
�ʴ�Ϊ��NaHCO3��4CO+3CO32-+5H2O=6HCO3-+CH4����
���� ���⿼�鷴Ӧ���йؼ��㡢ƽ�ⳣ������Ӱ�����ء���ѧƽ���Ӱ�����ء���ѧƽ��ͼ���ۺ�Ӧ�õȣ����ؿ���ѧ������������������Ҫѧ���߱���ʵ�Ļ������Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | CH4��C2H4��C3H4��������� | |
| B�� | CH4��C3H6��C2H2����C3H6��C2H2=1��2�����ʵ���֮�ȣ� | |
| C�� | CH4��C2H6��C3H8ͬ�����������Ϊ2��1��2 | |
| D�� | C2H4��C3H6��C4H8���������� |
| A�� | ���ǻ��Ϸ�Ӧ���Ƿ��ȷ�Ӧ���ֽⷴӦ�������ȷ�Ӧ | |
| B�� | �Ȼ�ѧ����ʽ�У����û��ע���¶Ⱥ�ѹǿ�����ʾ�ڱ�״���²�õ����� | |
| C�� | �Ȼ�ѧ����ʽ�У���ѧʽǰ��Ļ�ѧ�������ȿɱ�ʾ�������ֿɱ�ʾ���ʵ��� | |
| D�� | ��д�Ȼ�ѧ����ʽʱ������Ҫд����Ӧ�ȵķ��š���ֵ�͵�λ����Ҫע�������ʵľۼ�״̬ |
| A�� | ����ı�ȼ����Ϊ-890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| B�� | 500�桢30 Mpa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| C�� | ͬ��ͬѹ�£�H2��g��+Cl2��g��=2HCl��g���ڹ��պ͵�ȼ�����ġ�H��ͬ | |
| D�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3kJ/mol����H2SO4��Ca��OH��2��Ӧ���к��ȡ�H=2����-57.3��kJ/mol |
| A�� | ̼������Һ�Լ��ԣ���������Һ�����ԣ��ж�̼����ķǽ�����ǿ�� | |
| B�� | Cl2��Br2�ֱ��H2��Ӧ���ж�������ķǽ�����ǿ�� | |
| C�� | ��MgSO4��Al��NO3��3��Һ�зֱ��������İ�ˮ���ж�þ�����Ľ�����ǿ�� | |
| D�� | �ƺͼطֱ�����ˮ��Ӧ���ж��ƺͼصĽ�����ǿ�� |
