题目内容
【题目】(1)下列有关实验的叙述,错误的是(填序号)_______;
A 用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
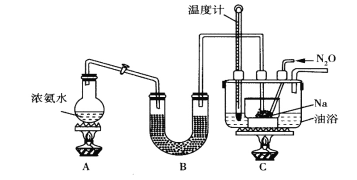
B 分馏石油时,温度计的末端必须插入液面下
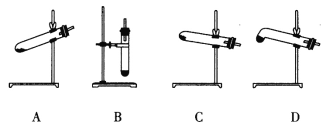
C 用分液漏斗分离环己烷和水的混合液体
D 用浓氨水洗涤做过银镜反应的试管
E 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
(2)人造羊毛在许多方面比天然羊毛更优良,其分子存在如下结构:
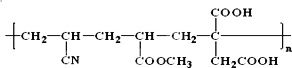
合成它的单体有_________。
(3)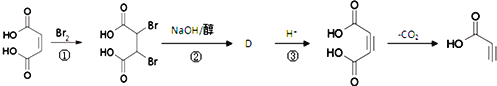
写出反应②的化学方程式 __________。
【答案】ABD CH2=CH﹣CN;CH2=CH﹣COOCH3;CH2=C(COOH)﹣CH2COOH 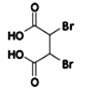 +4NaOH
+4NaOH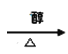
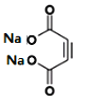 +2NaBr+4H2O
+2NaBr+4H2O
【解析】
根据物质的性质对有关实验的叙述进行分析;根据高聚物的结构特点分析单体结构;根据有机物的结构变化及反应条件分析发生的化学反应写出相应方程式。
(1)A.NaOH溶液能使乙酸乙酯水解,故A错误;
B.分馏石油时,温度计的末端应靠近蒸馏烧瓶的支管口处,故B错误;
C.环己烷和水不互溶且密度比水的密度要小,可以用分液漏斗分离环己烷和水的混合液体,故C正确;
D.银单质与氨水不反应,可用稀硝酸洗去,故D错误;
E.向硝酸银溶液中滴加氨水,等到白色沉淀恰好溶解时,可以获得银氨溶液,故E正确;
故选ABD。
(2)链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,结构简式中主链上有6个碳原子其单体必为3种,将双键中的3个C—C打开,然后将半键闭合即可得该高聚物单体是 CH2=CH﹣CN;CH2=CH﹣COOCH3;CH2=C(COOH)﹣CH2COOH;
(3)根据反应前后的结构变化及反应条件分析,反应②为消去反应,形成碳碳三键,同时结构中还含有羧基,与氢氧化钠发生中和反应,所以反应②的化学方程式为: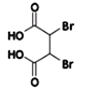 +4NaOH
+4NaOH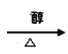
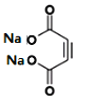 +2NaBr+4H2O。
+2NaBr+4H2O。

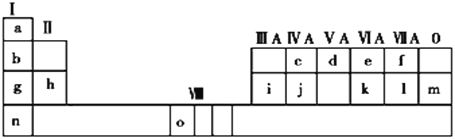
【题目】下表为元素周期表的一部分,请参照元素①——⑨在表中的位置,回答问题
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中⑧是用于半导体材料的元素,其元素符号为____,其在周期表中的位置是____。
(2)②、③、④的原子半径最小是____(填元素符号),其原子结构示意图是____。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是____(填化学式)。
(4)①和③形成的原子个数比为1:1的化合物的电子式为____。
(5)⑤和⑨形成的化合物属于____(填“离子化合物”或“共价化合物”),用电子式表示其形成过程____