题目内容
6.某同学欲配制符合下列条件的溶液,其中可能实现的是( )| A. | 只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液 | |
| B. | 只含0.1 mol NH4+、0.1 mol Ca2+、0.1 mol CO32-和0.1 mol Cl-的溶液 | |
| C. | 为了通过测定pH的大小,达到比较HCl和CH3COOH酸性强弱的目的,分别配制100 mL 0.1 mol/L的NaCl溶液和CH3COONa溶液 | |
| D. | 仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液 |
分析 A、从溶液要呈电中性角度来分析;
B、从离子共存角度来分析;
C、通过测定 0.1mol/L的NaCl溶液和CH3COONa溶液的pH的大小,可知HCl和CH3COOH酸性强弱;
D、定容时需要用胶头滴管.
解答 解:A、溶液要呈电中性,即阳离子所带的正电荷数要与阴离子所带的负电荷数相等,而只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液中,阳离子所带的正电荷的物质的量n=0.1mol+0.2mol×2=0.5mol,阴离子所带的负电荷的物质的量n=0.1mol+0.1mol=0.2mol,溶液不呈电中性,故A错误;
B、在溶液中,Ca2+和 CO32-不能共存,故B错误;
C、根据越弱越水解可知,酸越弱,对应的钠盐的碱性应越强,故可以通过测定 0.1mol/L的NaCl溶液和CH3COONa溶液的pH的大小,可知HCl和CH3COOH酸性强弱,故C正确;
D、配制1 L 1 mol/L的NaCl溶液在定容时需要用到胶头滴管,故D错误.
故选C.
点评 本题考查了溶液的电中性和离子共存以及盐的水解等问题,难度不大.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
17. 在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
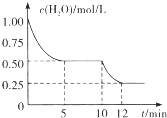
c( H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
 在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得c( H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
| A. | 0-5 min内,v(H2)=0.05 mol/(L.min) | |
| B. | 5 min时该反应的K值一定小于12 min时的K值 | |
| C. | 10 min时,改变的外界条件可能是减小压强 | |
| D. | 5 min时该反应的v正大于11 min时的v逆 |
14.下列说法或叙述不正确的是( )
| A. | 蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解 | |
| B. | 饱和(NH4)2SO4溶液能使蛋白质变性 | |
| C. | 用半透膜可除去蛋白质溶液中的NaCl | |
| D. | 用灼烧的方法检验是毛线还是棉线 |
1.下列说法正确的是( )
| A. | 可用如图所示装置作为实验室制取乙烯的发生装置 | |
| B. | 乙烯与酒精蒸汽按任意物质的量比混合,取VL该气体完全燃烧,相同条件消耗O2体积为3VL | |
| C. | 乙烯、乙醇都能使酸性高锰酸钾溶液褪色,符合通式CnH2n和CnH2n+2O的物质也都能使酸性高锰酸钾溶液褪色 | |
| D. | 甲苯在光照条件和 FeBr3作用下都能与Br2反应,反应产物相同 |
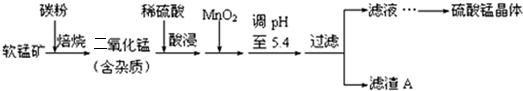
4.工业上利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰的常见流程如下:
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
(1)一氧化锰用硫酸酸浸时发生的主要反应的离子方程式为MnO+2H+=Mn2++H2O.酸浸后加入MnO2将溶液中的Fe2+氧化成Fe3+,其目的是确保铁元素在后续操作中完全转化为氢氧化物沉淀而除去.
(2)滤渣A的成分除MnO2外,还有Fe(OH)3和Al(OH)3.
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2.工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,当阴极产生4.48L(标况)气体时,MnO2的理论产量为17.4g.
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是Mn(OH)2>MnCO3>MnS(填写化学式).

部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 |
(2)滤渣A的成分除MnO2外,还有Fe(OH)3和Al(OH)3.
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2.工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,当阴极产生4.48L(标况)气体时,MnO2的理论产量为17.4g.
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是Mn(OH)2>MnCO3>MnS(填写化学式).
11.下列各组粒子中,所含化学键类型有差异的是( )
| A. | CCl4 和CH2Cl2 | B. | H3O+ 和NH4+ | C. | CaO2 和 CaF2 | D. | Ba(0H)2 和NaOH |
8.改变反应物的用量,下列反应不能用同一个反应方程式表示的是( )
①NaAlO2溶液与CO2反应; ②Si与烧碱溶液反应; ③H2S与NaOH溶液反应;
④Fe与稀硝酸反应; ⑤S在O2中燃烧; ⑥C与O2的反应.
①NaAlO2溶液与CO2反应; ②Si与烧碱溶液反应; ③H2S与NaOH溶液反应;
④Fe与稀硝酸反应; ⑤S在O2中燃烧; ⑥C与O2的反应.
| A. | ①②③⑤ | B. | ①③④ | C. | ①③④⑥ | D. | ①③④⑤⑥ |
9.向一定浓度的下列物质的澄清溶液中通入过量的CO2气体,最后肯定没有沉淀生成的是( )
①Ca(OH)2 ②Na2CO3 ③CaCl2 ④Ca(ClO)2 ⑤Na2SiO3.
①Ca(OH)2 ②Na2CO3 ③CaCl2 ④Ca(ClO)2 ⑤Na2SiO3.
| A. | ①③④ | B. | ②③④ | C. | ①②③⑤ | D. | ①②③④ |