题目内容
【题目】下列关于有机物的说法正确的是( )
A. CH3CH(C2H5)CH2CH(CH3)CH3的名称为2-甲基-4-乙基戊烷
B. ![]() 中至少有16个原子共平面
中至少有16个原子共平面
C. 分子式为C5H10O2的能够发生水解反应和银镜反应的有机物有8种
D. 淀粉和蛋白质水解的最终产物都只有一种
【答案】B
【解析】
A.CH3CH(C2H5)CH2CH(CH3)CH3的名称为2,4二甲基己烷,A错误;
B.由于苯分子是平面分子,处于苯环对位的两个碳原子在同一条直线上,一条直线上2点在一个平面上,则这条直线上所有的点都在这个平面上,所有![]() 中至少有16个原子共平面,B正确;
中至少有16个原子共平面,B正确;
C.分子式为C5H10O2的能够发生水解反应和银镜反应的有机物是甲酸形成的酯,具有HCOOC4H9结构,丁基有2种结构,每种结构有4种不同位置的H原子,所以—C4H9有8种不同结构,所以分子式为C5H10O2的能够发生水解反应和银镜反应的有机物有8种,C正确;
D.淀粉和蛋白质都是高分子化合物,淀粉水解最终产生葡萄糖,蛋白质是由多种氨基酸发生缩聚反应形成,因此蛋白质发生水解反应,最终也会得到多种氨基酸,D错误;
故合理选项是B。

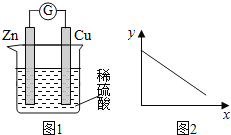
【题目】Ⅰ:用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:

实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
② | 20 mL 0.2 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
(1)该实验探究的是_________________________________因素对化学反应速率的影响。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________ mol·L-1(假设混合溶液的体积为50 mL)。
(3)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:
①产物Mn2+是反应的催化剂,②_______________________________
Ⅱ:当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式为___________________________________
(2)在恒温恒容密闭容器中,判断上述反应达到平衡状态的依据是________________
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1