题目内容
【题目】原电池的发明是化学对人类的一项重大贡献。依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+设计的原电池如图所示。
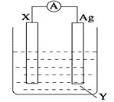
(1)电极X的材料是__;电解质溶液Y是__。
(2)Ag电极上发生的反应为:__。
【答案】Cu Fe2(SO4)3或FeCl3 Fe3++e-=Fe2+
【解析】
(1)依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+,负极金属材料是Cu,电解质是含有铁离子的盐溶液;
(2)原电池的正极得电子,发生还原反应,负极失电子,发生氧化反应,结合电子守恒、电荷守恒写出电极反应式。
(1)依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+,负极金属材料是Cu,所以电极X的材料是Cu,电解质Y是含有铁离子的盐溶液,可以是Fe2(SO4)3溶液或FeCl3溶液,故答案为:Cu;Fe2(SO4)3或FeCl3;
(2)原电池的正极是银电极,铁离子得电子,发生还原反应,即Fe3++e-=Fe2+,故答案为:Fe3++e-=Fe2+。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目