题目内容
2.金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).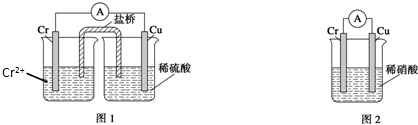
(1)铜铬构成原电池如图1,其中盛稀硫酸烧杯中的现象为:铜电极上有气泡产生.盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是B
A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
(2)如构成图2电池发现,铜电极上不再有图1的现象,铬电极上产生大量气泡,遇空气呈红棕色.写出正极电极反应式:4H++NO3-+3e-=NO↑+2H2O.
分析 (1)铬能与稀硫酸反应,生成氢气;
A、盐桥中不是都可以用饱和KCl琼脂溶液,要考虑能否与电解质溶液反应;
B、1molCr反应,转移2mol电子;
C、氢离子得电子发生还原反应;
D、盐桥中是离子移动,无电子通过;
(2)正极上是硝酸根离子得电子生成NO,结合电荷守恒和原子守恒书写电极反应式.
解答 解:(1)铬能与稀硫酸反应生成氢气,盛稀硫酸烧杯中在铜电极上有气泡产生;
A、盐桥中不是都可以用饱和KCl琼脂溶液,若电解质溶液为硝酸银溶液时,会生成沉淀,故A错误;
B、1molCr反应,转移2mol电子,为保持电荷守恒,盐桥中将有2molCl-进入左池,2molK+进入右池,故B正确;
C、氢离子得电子发生还原反应,故C错误;
D、盐桥中是离子移动,无电子通过,故D错误;
故答案为:铜电极上有气泡产生;B;
(2)正极上是硝酸根离子得电子生成NO,有氢离子参与反应,电极反应式为:4H++NO3-+3e-=NO↑+2H2O,故答案为:4H++NO3-+3e-=NO↑+2H2O;
点评 本题考查了原电池原理、盐桥原理、电极反应式书写等,题目难度较大,注意电解质溶液中无电子的移动.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
12.下列说法正确的是( )
| A. | 摩尔是国际七个基本物理量之一 | |
| B. | 摩尔质量等于相对分子质量或相对原子质量 | |
| C. | 标准状况下,任何气体的摩尔体积都约为22.4L | |
| D. | 1mol某种微粒含有的微粒数等于0.012kg12C所具有的碳原子数 |
13.下列实验不能获得成功的为( )
①用酸性KMnO4溶液除C2H6中混有的CH2=CH2
②将乙醇与浓硫酸缓慢加热让温度慢慢升至170℃制取乙烯
③在电石中加水制取乙炔
④苯、浓溴水和铁粉混和,反应制溴苯
⑤将苯、浓硝酸、浓硫酸混合制TNT.
①用酸性KMnO4溶液除C2H6中混有的CH2=CH2
②将乙醇与浓硫酸缓慢加热让温度慢慢升至170℃制取乙烯
③在电石中加水制取乙炔
④苯、浓溴水和铁粉混和,反应制溴苯
⑤将苯、浓硝酸、浓硫酸混合制TNT.
| A. | ②⑤ | B. | ①②⑤ | C. | ①②④⑤ | D. | ②④ |
10.下列说法错误的是( )
| A. | 化合反应不一定是氧化还原反应 | |
| B. | 置换反应一定是氧化还原反应 | |
| C. | 氧化还原反应中,非金属单质一定是氧化剂 | |
| D. | 氧化还原反应中,金属单质一定是还原剂 |
7.对于化学式为C5H12O2的二元醇,其主链为4个碳原子的同分异构体有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
14.铁在一定条件下与O2,水蒸气反应的共同产物是( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | Fe(OH)3 |
8.在下列各说法中,正确的是( )
| A. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 | |
| D. | 1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |

 )就是其中的一种.
)就是其中的一种.