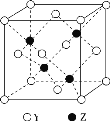
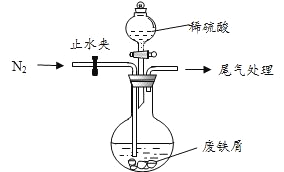
题目内容
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取金属铝的生产过程如下框图
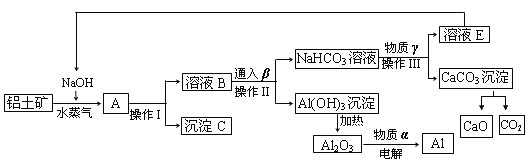
请回答下列问题:
(1)纯净的氧化铝俗称____________,属于____________晶体。写出铝土矿与氢氧化钠溶液反应的离子方程式_______________。
(2)沉淀C的化学式为______,该物质除了用于金属冶炼以外,还可用作______________。电解熔融的氧化铝时,物质α是______,其作用是_________________。
(3)在实验室中欲从溶液E中得到较纯净的固体NaOH,需要进行的操作顺序是:_______、趁热过滤、____、__________。
(4)生产过程中,可以循环使用的物质有四种,除NaOH、H2O、CaO、CO2。其中NaOH中含有的化学键是______、________(如有共价键须标明极性还是非极性)。CaO、CO2的电子式分别为_____、____。
【答案】刚玉 原子 Al2O3+ OH-→ 2AlO2-+ H2O Fe2O3 颜料 冰晶石 熔剂(使Al2O3易熔融) 加热浓缩或蒸发浓缩 冷却结晶 过滤洗涤 离子键 共价键 ![]()
![]()
【解析】
铝土矿中含有氧化铝和氧化铁,向铝土矿中加入NaOH溶液,发生反应Al2O3 + 2OH-=2AlO2- + H2O、Al2O3+2OH-═2AlO2-+H2O,氧化铁不溶于NaOH溶液,然后过滤,得到溶液B为NaOH、NaAlO2混合溶液,沉淀C为Fe2O3,向溶液B中通入CO2,发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、2OH-+CO2=CO32-+H2O,然后过滤得到沉淀Al(OH)3和NaHCO3溶液,向溶液中加入CaO,发生反应NaHCO3+CaO═NaOH+CaCO3↓,然后过滤,将NaOH循环利用;将Al(OH)3加热得到Al2O3,电解熔融Al2O3得到Al,以此解答该题。
(1)纯净的氧化铝俗称刚玉,是原子晶体。铝土矿含氧化铝、氧化铁,氧化铝是两性氧化物,既可与酸反应又可与碱反应,只有氧化铝与氢氧化钠反应,方程式为Al2O3 + OH-=2AlO2- + H2O
故答案为:刚玉;原子;Al2O3 + OH-=2AlO2- + H2O;
(2)由以上分析可知沉淀C为Fe2O3,可用于做颜料;氧化铝的熔点比较高,电解熔融的氧化铝时,需加入冰晶石,降低它的熔点,物质α是冰晶石,作用是降低氧化铝的熔点,即做熔剂(使Al2O3易熔融);
故答案为:Fe2O3;颜料;冰晶石;熔剂(使Al2O3易熔融);
(3)从溶液中得到氢氧化钠晶体,可加热浓缩或蒸发浓缩,然后趁热过滤,冷却结晶并过滤洗涤,
故答案为:加热浓缩或蒸发浓缩;冷却结晶;过滤洗涤;
(4) NaOH属于强碱,是离子晶体,主要含有离子键,OH-中氢和氧原子之间共用一对用用电子对,存在共价键,氢和氧电负性不同,吸引共用电子对的能力也不能,故共用电子对有偏移,是极性共价键,CaO是活泼金属氧化物,含有离子键,是离子晶体,故电子式为![]() ,CO2是共价化合物,,碳的最外层有四个电子,与氧各形成两对共用电子对,故电子式为
,CO2是共价化合物,,碳的最外层有四个电子,与氧各形成两对共用电子对,故电子式为![]() ,
,
故答案为:离子键;共价键;![]() ;
;![]() 。
。

【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是___(填编号),该错误操作会导致测定结果___(填“偏大”、“偏小”或“无影响”)。
(2)实验中用左手控制___,眼睛注视___,直至滴定终点。判断滴定终点的现象是:锥形瓶中溶液___。
(3)如图是某次滴定时的滴定管中的液面,其读数为___mL。
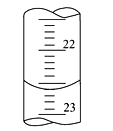
(4)根据下列数据:请计算待测盐酸溶液的浓度为___mol/L。
滴定次数 | 待测液体积(mL) | 标准液读数记录(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.42 | 20.40 |
第二次 | 20.00 | 2.28 | 22.30 |
第三次 | 20.00 | 0.20 | 22.60 |
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的X值。
元素 | Li | Be | B | C | O | F |
X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
元素 | Na | Al | Si | P | S | Cl |
X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析X值的变化规律,确定N、Mg的X值范围:___<X(Mg)<___;___<X(N)<___。
(2)推测X值与原子半径的关系是___。
(3)某有机物结构简式为![]() ,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是_______。
(5)预测元素周期表中,X值最小的元素位置_______(放射性元素除外)。