题目内容
11.V、W、X、Y、Z是原子序数依次递减的五种常见元素.X元素是地壳中含量最多的元素,Y、Z组成气态化合物M的水溶液呈碱性,W的单质在X2中燃烧的产物可使品红溶液褪色,V是一种历史悠久,应用广泛的金属元素.请回答:(1)Y元素在周期表中的位置是第二周期第ⅤA族;写出X、Z两种元素组成的化合物Z2X2一种用途:消毒剂或氧化剂或漂白剂.
(2)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且属于氧化还原反应,请写出该反应的化学方程式3NO2+H2O=2HNO3+NO.
(3)X、Y、Z三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐.常温下该盐的水溶液的pH小于7(填“大于”、“小于”或“等于”).
(4)W(s)+O2(g)═WO2(g);△H1
W(g)+O2(g)═WO2(g);△H2
则△Hl>△H2(填“>”或“<”或“=”)
(5)有人设想寻求合适的催化剂和电极材料,以Y2、Z2为电极反应物,以HCl一NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式N2+8H++6e-=2NH4+;放电时溶液中H+移向正(填“正”或“负”)极.
(6)若将V金属投入到硫酸溶液中,生成了浅绿色溶液N.写出N的溶液与K2Cr2O7酸性的溶液反应的离子方程式:6Fe2++Cr2O72-+14H+=6 Fe3++2Cr3++7H2O.
分析 V、W、X、Y、Z是原子序数依次递减的五种常见元素.X元素是地壳中含量最多的元素,则X为O元素;Y、Z组成的气态化合物M的水溶液呈碱性,可推知Y为N元素、Z为H元素,M为NH3;W的单质在X2中燃烧产物可使品红溶液褪色,可推知W为S元素;V是一种历史悠久、应用最广泛的金属元素,则V为Fe元素,据此解答.
解答 解:V、W、X、Y、Z是原子序数依次递减的五种常见元素.X元素是地壳中含量最多的元素,则X为O元素;Y、Z组成的气态化合物M的水溶液呈碱性,可推知Y为N元素、Z为H元素,M为NH3;W的单质在X2中燃烧产物可使品红溶液褪色,可推知W为S元素;V是一种历史悠久、应用最广泛的金属元素,则V为Fe元素.
(1)Y为N元素,在周期表中的位置是:第二周期第ⅤA族;化合物H2O2可以用作消毒剂、氧化剂、漂白剂,
故答案为:第二周期第ⅤA族;消毒剂或氧化剂或漂白剂;
(2)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且反应属于氧化还原反应,应是二氧化氮与水反应生成硝酸与NO,该反应的化学方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
(3)O、N、H三种元素可组成一种强酸U为HNO3,氨气在适当条件下被HNO3吸收生成NH4NO3,该盐的水溶液中NH4+离子水解:NH4++H2O?NH3.H2O+H+,破坏水的电离平衡,溶液呈酸性,溶液pH小于7,
故答案为:小于;
(4)已知:①S(s)+O2(g)═SO2(g)△H1
②S(g)+O2(g)═SO2(g)△H2
根据盖斯定律,①-②可得:S(s)=S(g)△H=△H1-△H2,气态硫的能量高于固态硫,故△H1-△H2>0,即△Hl>△H2,
故答案为:>;
(5)以N2、H2为电极反应物,以HCl-NH4Cl溶液为电解质溶液制造新型燃料电池,正极发生还原反应,氮气在正极获得电子,酸性条件下生成NH4+,该电池的正极电极反应式为:N2+8H++6e-=2NH4+,放电时溶液中H+向正极移动,
故答案为:N2+8H++6e-=2NH4+;正;
(6)将Fe投入到硫酸溶液中,生成了浅绿色FeSO4溶液,K2Cr2O7酸性的溶液具有强氧化性,将亚铁离子氧化为铁离子,自身还原得到Cr3+,同时生成水,反应的离子方程式为:6Fe2++Cr2O72-+14H+=6 Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+=6 Fe3++2Cr3++7H2O.
点评 本题考查结构性质位置关系应用,题目难度中等,推断元素的种类是关键,需要学生具备扎实的基础,注意电极反应式的书写.

| A. | 乙醇、乙二醇、丙三醇互为同系物;H2、D2、T2互为同素异形体 | |
| B. | 绿矾、碱石灰、苏打、干冰分别属于纯净物、混合物、电解质、非电解质 | |
| C. | 乙烯水化、铁铝钝化、植物油氢化、纯碱晶体风化等过程中都包含化学变化 | |
| D. | 蛋白质、纤维素、硝化纤维等都是高分子化合物 |
| A. | 除去NaHCO3溶液中少量的Na2CO3:加入适量稀盐酸 | |
| B. | 除去FeCl2溶液中少量的FeCl3:加入稍过量铁粉,过滤 | |
| C. | 除去NH4Cl固体中少量I2:加热,I2升华除去 | |
| D. | 除去乙烯中的少量SO2:通过酸性KMnO4溶液,洗液 |
| A. | n(NO2-)+n(OH-)-n(H+)=0.1 mol | |
| B. | 若加入少量CH3COONa固体,溶液的碱性会减弱 | |
| C. | 若再通入0.01 mol HCl气体,溶液pH大于2(忽略溶液体积的变化) | |
| D. | 此时溶液的pH大于0.1 mol•L-1的CH3COONa溶液 |
 .
.  .
.  .
. 和其他无机物叫合成
和其他无机物叫合成 ,最合理的方案
,最合理的方案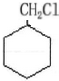 $→_{△}^{NaOH、醇}$
$→_{△}^{NaOH、醇}$ $\stackrel{Cl_{2}}{→}$
$\stackrel{Cl_{2}}{→}$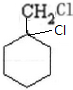
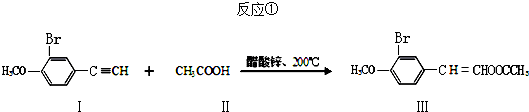
 (任写其中一种)
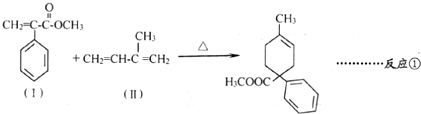
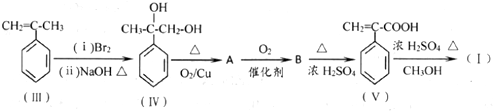
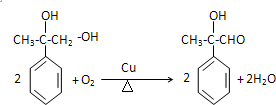
(任写其中一种) 涂料的单体,化合物Ⅴ单体结构简式为CH3COOCH=CHCH3.
涂料的单体,化合物Ⅴ单体结构简式为CH3COOCH=CHCH3. .利用类似反应①的方法,仅以丙炔和乙酸为有机物原料合成该单体,写出反应方程式
.利用类似反应①的方法,仅以丙炔和乙酸为有机物原料合成该单体,写出反应方程式 .
.
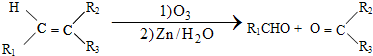
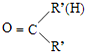 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$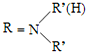 +H2O
+H2O +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O
+H2O
 .(写出其中的一种的结构简式).
.(写出其中的一种的结构简式). $\stackrel{反应条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件下}^{C}$J$\stackrel{还原}{→}$
$\stackrel{反应条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件下}^{C}$J$\stackrel{还原}{→}$
 .
.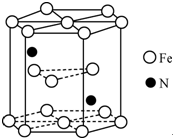 铁及其化合物在生产生活及科学研究方面应用非常广泛.
铁及其化合物在生产生活及科学研究方面应用非常广泛. .
.