题目内容
16.用NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 0.1mol•L-1稀硫酸100mL中含有硫酸根个数为0.1NA | |
| B. | 1mol CH3+(碳正离子)中含有电子数为10NA | |
| C. | 2.4g金属镁与足量的盐酸反应,转移电子数为2NA | |
| D. | 12.4g白磷中含有磷原子数为O.4NA |
分析 A、根据n=CV来计算;
B、根据CH3+(碳正离子)显正电性来计算;
C、求出镁的物质的量,然后根据反应后镁的价态为+2价来分析;
D、根据n=$\frac{m}{M}$来计算.
解答 解:A、0.1mol/L100mL稀硫酸中含有硫酸根的物质的量n=CV=0.1mol/L×0.1L=0.01mol,故个数为0.01NA,故A错误;
B、CH3+(碳正离子)显正电性,1molCH3+(碳正离子)中含有电子数为8NA,故B错误;
C、2.4g镁的物质的量为0.1mol,而反应后镁的价态为+2价,故0.1mol镁失去0.2mol电子即0.2NA个,故C错误;
D、12.4g白磷中含有磷原子数为=$\frac{12.4g}{31g/mol}{N}_{A}/mol$=0.4NA,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.常温下,将盐酸和一元碱BOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
根据实验结果,回答下列问题:
(1)试写出BOH在溶液中的电离方程式:BOH?B++OH-
(2)甲组混合溶液中离子浓度由大到小的顺序为:c(Cl-)>c(B+)>c(H+)>c(OH-)
(3)乙组混合溶液中B-离子浓度c(B-)=0.05 mol/L
(4)丙组混合溶液中c(BOH)、c(B-)、c(Cl-)浓度大小关系为c(BOH)>c(B+)>c(Cl-)
(5)根据乙组实验,列式并计算BOH在常温下的电离平衡常数Kb=5×10-8.
| 实验序号 | HCl溶液浓度(mol/L) | BOH溶液溶液(mol/L) | 混合后溶液pH |
| 甲 | 0.10 | 0.10 | 4.7 |
| 乙 | 0.10 | 0.30 | 7 |
| 丙 | 0.10 | 0.50 | 8.2 |
(1)试写出BOH在溶液中的电离方程式:BOH?B++OH-
(2)甲组混合溶液中离子浓度由大到小的顺序为:c(Cl-)>c(B+)>c(H+)>c(OH-)
(3)乙组混合溶液中B-离子浓度c(B-)=0.05 mol/L
(4)丙组混合溶液中c(BOH)、c(B-)、c(Cl-)浓度大小关系为c(BOH)>c(B+)>c(Cl-)
(5)根据乙组实验,列式并计算BOH在常温下的电离平衡常数Kb=5×10-8.
1.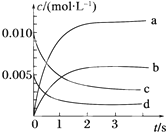 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为65%.用O2表示从0~2s内该反应的平均速率v=0.0015mol/(L•s).
(2)如图所示,表示NO2变化曲线的是b.
(3)能说明该反应已达到平衡状态的是bc(填序号).
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,表示NO2变化曲线的是b.
(3)能说明该反应已达到平衡状态的是bc(填序号).
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
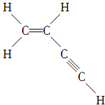 则分子中有7个 σ 键,3个 π 键.
则分子中有7个 σ 键,3个 π 键. .若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯,结构简式是(CH3)3C-CH=CH2.比烃A少两个碳原子且能使溴水褪色的A的同系物有3种同分异构体.
.若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯,结构简式是(CH3)3C-CH=CH2.比烃A少两个碳原子且能使溴水褪色的A的同系物有3种同分异构体.
 .
. .
. .
.