题目内容
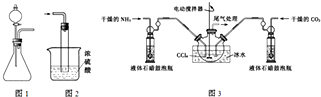
4.工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程.
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则整个装置气密性良好.装置D的作用是防止倒吸.装置E中为NaOH溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为2:1.
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度.已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是溶液变澄清(或浑浊消失).反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有ad.
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:取少量产品溶于足量稀盐酸、静置、取上层清液(或过滤,取滤液)、滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质.
已知Na2S2O3•5H2O遇酸易分解:S2O32-+2H+═S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
分析 (1)液柱高度保持不变,说明气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用;
(2)根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3;
(3)观察SO2的生成速率,发生强酸制取弱酸的反应,Ⅲ中发生S(g)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq),反应达到终点是S完全溶解,烧杯、锥形瓶需要加热时必须使用石棉网,蒸发皿、试管可直接加热;
(4)加入盐酸,Na2S2O3反应生成S沉淀,所以静置后取上层清液,滴加BaCl2溶液,检验溶液中是否含有硫酸根离子;
解答 解:(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变;防止倒吸;NaOH;
(2)根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)观察SO2的生成速率,发生强酸制取弱酸的反应,a不生成二氧化硫,bd中物质均与二氧化硫反应,只有c中饱和NaHSO3溶液适合制取二氧化硫;Ⅲ中发生S(g)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq),反应达到终点是S完全溶解,可观察到溶液变澄清(或浑浊消失);烧杯、锥形瓶需要加热时必须使用石棉网,
故答案为:c;控制滴加硫酸的速度;溶液变澄清(或浑浊消失);ad;
(4)检测产品中是否存在Na2SO4的实验方案为:取少量产品溶于足量稀盐酸、静置、取上层清液(或过滤,取滤液)、滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸、静置、取上层清液(或过滤,取滤液)、滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
点评 本题考查实验方案的分析与评价,涉及气密性检验、离子检验、对操作的分析评价、化学计算等,侧重实验分析能力及知识综合应用能力的考查,(2)为易错点,可以利用总反应的分析,题目难度中等.

| A. | 0.1mol•L-1稀硫酸100mL中含有硫酸根个数为0.1NA | |
| B. | 1mol CH3+(碳正离子)中含有电子数为10NA | |
| C. | 2.4g金属镁与足量的盐酸反应,转移电子数为2NA | |
| D. | 12.4g白磷中含有磷原子数为O.4NA |
| A. | pH=2的HA溶液与pH=12的MOH溶液等体积混合后pH<7,则HA为弱酸 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| C. | 物质的量浓度均为0.2mol•L-1CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COO-)+c(CH3COOH)=0.2mol•L-1 | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| A. | 1:2 | B. | 2:3 | C. | 3:2 | D. | 1:1 |
| A. | CH2Cl2有 和 和 两种结构 两种结构 | |
| B. | 烯烃跟氢气起加成反应产物是2,2,3,4-四甲基戊烷,则这样的烯烃有3种 | |
| C. | 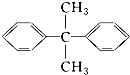 的一氯代物有5种 的一氯代物有5种 | |
| D. | 1 mol某烷烃完全燃烧消耗11 mol O2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有6种 |
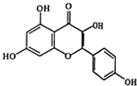 山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )
山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )| A. | 结构式中含有2个苯环和羟基、醚键、羧基、碳碳双键 | |
| B. | 可发生取代反应、水解反应、加成反应 | |
| C. | 可与NaOH反应,不能与NaHCO3反应 | |
| D. | 1mol山萘酚与溴水反应最多可消耗4molBr2 |
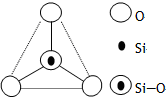 如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )
如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )| A. | 键角为120℃ | B. | 化学组成为SiO32- | ||
| C. | 键角为60° | D. | 化学组成为SiO44- |