题目内容
【题目】合成神经抑制剂F的一种路线如图所示:
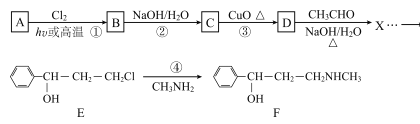
已知:![]()
请回答下列问题:
(1)已知芳香烃A的相对分子质量为92,A的结构简式为____;B的系统命名是___ ;C中含氧官能团的名称是____。
(2)反应③的化学反应方程式为____;①~④中属于取代反应的是____。
(3)D分子中最多有____个原子共平面。
(4)④的反应中,因反应温度控制不当,常常有副产物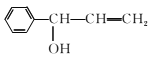 生成,写出可能的副反应方程式____。
生成,写出可能的副反应方程式____。
(5)包含C在内,C的同分异构体中芳香族化合物共有____种,其中满足下列条件同分异构体的结构简式为____。
①能使FeCl3溶液显色,②核磁共振氢谱上有4组峰,且峰面积之比为3:2:2:1。
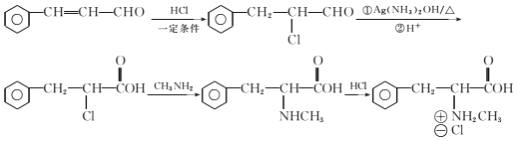
(6)已知-CHO与RNH2易发生反应,现以中间体X为原料,设计出制备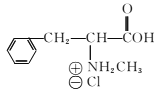 的合成路线(无机试剂自选):________________________________________
的合成路线(无机试剂自选):________________________________________
流程示例:![]()
【答案】 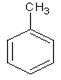 1-氯甲苯 羟基或醇羟基
1-氯甲苯 羟基或醇羟基 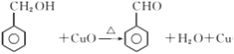 ①②④ 14
①②④ 14 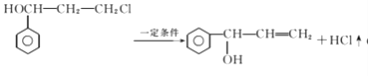 5
5 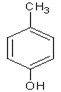
【解析】A为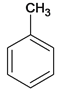 ,光照条件下与氯气在侧链上取代得B
,光照条件下与氯气在侧链上取代得B ,B在氢氧化钠加热条件下水解生成C
,B在氢氧化钠加热条件下水解生成C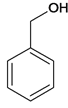 ,C氧化成D
,C氧化成D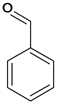 。
。
(1)芳香烃A的相对分子质量为92,92/12=7...8,A的分子式为C7H8,A的结构简式为 ;B
;B 的系统命名是1-氯甲苯 ;C
的系统命名是1-氯甲苯 ;C 中含氧官能团的名称是 羟基或醇羟基;(2)反应③是醇氧化成醛,化学反应方程式为
中含氧官能团的名称是 羟基或醇羟基;(2)反应③是醇氧化成醛,化学反应方程式为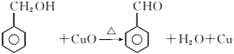 ;①~④中③是氧化反应,属于取代反应的是①②④;(3)D
;①~④中③是氧化反应,属于取代反应的是①②④;(3)D 分子中7C、6H和1个O原子,最多有14个原子共平面。(4)④的反应中,因反应温度控制不当,常常有副产物
分子中7C、6H和1个O原子,最多有14个原子共平面。(4)④的反应中,因反应温度控制不当,常常有副产物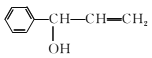 生成,写出可能的副反应方程式
生成,写出可能的副反应方程式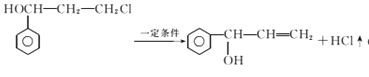
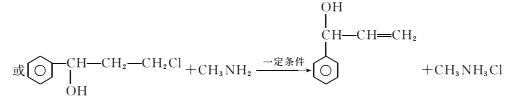 ;(5)包含C
;(5)包含C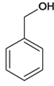 在内,C的同分异构体中芳香族化合物,有邻、间、对甲基苯酚3种,苯甲醚1种,苯甲醇1种,共有5种,其中满足①能使FeCl3溶液显色,有酚羟基,②核磁共振氢谱上有4组峰,且峰面积之比为3:2:2:1条件的结构简式:
在内,C的同分异构体中芳香族化合物,有邻、间、对甲基苯酚3种,苯甲醚1种,苯甲醇1种,共有5种,其中满足①能使FeCl3溶液显色,有酚羟基,②核磁共振氢谱上有4组峰,且峰面积之比为3:2:2:1条件的结构简式:![]() 。(6)已知-CHO与RNH2易发生反应,现以中间体X为原料,设计出制备
。(6)已知-CHO与RNH2易发生反应,现以中间体X为原料,设计出制备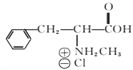 的合成路线:
的合成路线: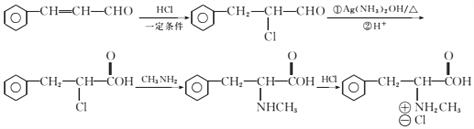 。
。