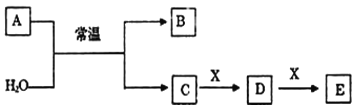
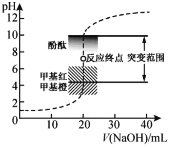
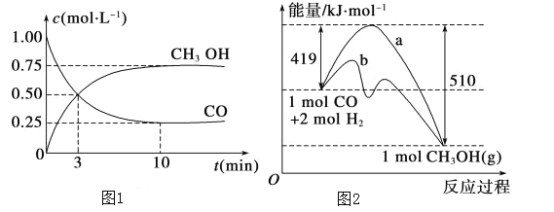
题目内容
【题目】碳及其化合物在生产和生活中有重要意义。海水中CO2的吸收能力取决于溶解的碳酸盐和硼酸盐生成的CO32-和B(OH)4-浓度。已知:298K时,H3BO3+H2O![]() H++B(OH)4-,Ka=5.7×10-10,碳酸的电离平衡常数:Ka1=4.3×10-7;Ka2=5.6×10-11
H++B(OH)4-,Ka=5.7×10-10,碳酸的电离平衡常数:Ka1=4.3×10-7;Ka2=5.6×10-11
(1)298K时,相同浓度的碳酸钠溶液和硼酸钠溶液,pH较大的是_______溶液。
(2)少量CO2与B(OH)4-反应的离子方程式为___________。
(3)采用高温熔融混合碳酸盐LiaNabKcCO3作电解质吸收并电解CO2制得无定型炭是CO2 资源化利用的一种新途径。此法的阴极电极反应式为________。
【答案】碳酸钠 CO2+B(OH)4-=HCO3-+H3BO3 3CO2+4e-=C+2CO32-
【解析】
(1)根据形成盐的酸的酸性越弱,等浓度时相应的酸根离子水解程度越大,溶液的碱性越强分析;
(2)根据复分解反应规律书写离子方程式;
(3)电解吸收CO2,在阴极CO2得到电子变为C单质,同时产生CO32-,据此书写阴极电极反应式。
(1)根据电离平衡常数大小可知:酸性:H2CO3>H3BO3>HCO3-,所以在298K时,相同浓度的碳酸钠溶液和硼酸钠溶液,CO32-水解程度比较大,最终达到平衡时溶液pH较大的是碳酸钠;
(2)由于酸性:H2CO3>H3BO3>HCO3-,少量CO2与B(OH)4-反应的离子方程式为CO2+B(OH)4-=HCO3-+H3BO3;
(3)采用高温熔融混合碳酸盐LiaNabKcCO3作电解质,吸收并电解CO2制得无定型炭是CO2 资源化利用的一种新途径,此法中CO2在阴极得到电子变为C单质,同时得到CO32-,阴极电极反应式为3CO2+4e-=C+2CO32-。

 阅读快车系列答案
阅读快车系列答案