题目内容
【题目】如图为铝热反应的实验装置,请回答下列问题:

(1)该实验装置中还缺________,引发铝热反应的操作为_______。
(2)若将氧化铁换成氧化镁,该反应____(填“能”或“不能”)发生,理由是______。
(3)铝热反应的用途有哪些__________。
【答案】镁条和氯酸钾 在混合物中间插一根镁条,将氯酸钾放在混合物上镁条的周围,点燃镁条 不能 镁比铝活泼,铝不能置换镁 用于焊接钢轨;冶炼某些熔点高的金属
【解析】
(1)利用镁条燃烧放热从而引发铝热反应,同时促使KClO3分解产生O2,使镁条快速燃烧。
(2)根据金属活动顺序表,Mg比Al活泼,Al不能从MgO中置换出Mg。
(1)实验需要的药品主要是镁条、氯酸钾、氧化铁、铝粉、细沙,因此该实验装置中还缺镁条和氯酸钾,引发铝热反应的操作为在混合物中间插一根镁条,将氯酸钾放在混合物上镁条的周围,点燃镁条,故答案为:镁条和氯酸钾;在混合物中间插一根镁条,将氯酸钾放在混合物上镁条的周围,点燃镁条。
(2)铝热反应是铝和金属氧化物(还原性比铝弱的金属氧化物)若将氧化铁换成氧化镁,该反应不能发生,理由是镁比铝活泼,铝不能置换镁,故答案为:不能;镁比铝活泼,铝不能置换镁。
(3)铝热反应的用途有哪些用于焊接钢轨;冶炼某些熔点高的金属,故答案为: 用于焊接钢轨;冶炼某些熔点高的金属。

【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
已知:Cr2O72-(aq)(橙色)+H2O(l) | |
步骤: | 现象: 待试管b中颜色不变后与试管a比较, 溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高, 溶液颜色与试管a相比,变深。 |
A. 该反应是一个氧化还原反应
B. 待试管b中溶液颜色不变的目的是使Cr2O72-完全反应
C. 该实验不能证明减小生成物浓度,平衡正向移动
D. 试管c中的现象说明影响平衡的主要因素是温度
【题目】通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H)。
化学键 | Cl-Cl | H—H | H—Cl | N≡N |
键能/kJ·mol | 243 | 436 | 431 | 946 |
(1)按要求完成填空
a.2HCl(g) = H2(g)+Cl2(g);△H=______________________
b.N2 (g)+3H2(g)= 2NH3(g) ΔH=-92kJ/mol,则N—H键的键能是__________kJ·mol
(2)1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式__________________________________

(3) 已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2
③ H2O(g) = H2O(l) ΔH3
则CH3OH(l)+O2(g)=CO(g)+ 2H2O(l)ΔH =__________(用含ΔH1、ΔH2、ΔH3的式子表示)
(4)已知:2Al (s)+ 3/2O2(g)==Al2O3(s) △H=-1644.3 kJ mol-1
2Fe (s) +3/2O2(g)==Fe2O3(s) △H=-815.88kJ mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式_______________________。
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是_______,占据该能层电子的电子云轮廓图形状为______________。
(2)已知元素M是组成物质![]() 的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号
的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号![]() 至
至![]() 表示)如表所示:
表示)如表所示:
|
|
|
|
| |
电离能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是_________价,其基态原子电子排布式为_______
(3)![]() 的中心原子的杂化方式为__________,键角为____________
的中心原子的杂化方式为__________,键角为____________
(4)![]() 中非金属元素电负性由大到小的顺序为_____________
中非金属元素电负性由大到小的顺序为_____________
(5)下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:![]() B.共价键的极性:
B.共价键的极性:![]()
C.晶格能:![]() D.热稳定性:
D.热稳定性:![]()
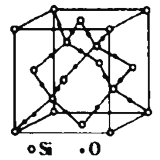
(6)如图是![]() 晶胞,构成二氧化硅晶体结构的最小环是由________个原子构成。已知晶胞参数为
晶胞,构成二氧化硅晶体结构的最小环是由________个原子构成。已知晶胞参数为![]() ,则其晶胞密度为________
,则其晶胞密度为________![]() 。
。