题目内容
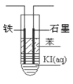
【题目】用苯和浓硝酸、浓硫酸按照如图装置制取硝基苯,回答下列问题:

(1)在配制混合酸时应将___________加入到___________中去;
(2)被水浴加热的试管口处都要带一长导管,其作用___________。
(3)该反应的化学方程式是___________;反应类型:___________。
(4)此装置存在几处错误,请修改(可不必填满).①______;②______;
③________。
(5)请从下列操作:①蒸馏;②水洗;③用干燥剂干燥;
④用10%NaOH溶液洗;⑤水洗,选择合适操作,进行分离混酸后的粗产品精制:分液________分液________分液________过滤________。(用序号表示)
【答案】(1)浓硫酸,浓硝酸;
(2)使苯蒸气冷凝回流,减少挥发
(3)![]() ;取代反应(硝化反应)
;取代反应(硝化反应)
(4)①温度计没有插在烧杯中的热水中;②导管太短;③试管碰到烧杯底部;
(5)②④⑤③①
【解析】试题分析:(1)浓硝酸的密度小于浓硫酸的密度,因此两种酸混合时,把浓硫酸慢慢加入到浓硝酸中,边加边搅拌;
(2)玻璃管的作用是使挥发出的反应物得到冷凝并使其回流到反应管中,即使苯蒸气冷凝回流,减少挥发。
(3)苯和浓硝酸发生硝化反应,硝基取代苯环上的一个氢原子,该反应为取代反应,反应方程式为:![]() ;
;
(4)①温度计测热水的温度,所以错误之处是温度计没有插在烧杯中的热水中;②玻璃管的作用是使挥发出的反应物得到冷凝并使其流回到反应管中,即起冷凝回流作用,所以玻璃管不能太短;③烧杯底部温度较高,反应温度应在 60℃,所以试管不能接触烧杯底部。
(5)硝基苯中混有混合酸,先用水洗,除去大部分混合酸,然后用 10%NaOH洗涤,除去剩下的酸,然后再用水洗,除去碱,接着用干燥剂除去水,最后蒸馏得到溴苯,正确的顺序是②④⑤③①。