题目内容
5.下列有关碱金属的说法中,不正确的是( )| A. | IA族元素都是碱金属元素 | B. | K的还原性强于Na | ||
| C. | Na和Na+灼烧时都能使火焰呈黄色 | D. | Na在空气中燃烧时生成Na2O2 |
分析 A.氢是非金属;
B.同主族元素从上到下单质的还原性依次增强;
C.焰色反应属于元素的性质;
D.钠在氧气中燃烧生成过氧化钠.
解答 解:A.IA族元素除去氢都是碱金属,故A错误;
B.钾与钠属于同主族,排在钠的下面,还原性强于Na,故B正确;
C.钠元素灼烧产生黄色火焰,故C正确;
D.钠在氧气中燃烧生成过氧化钠,故D正确;
故选:A.
点评 本题考查了碱金属的性质,熟悉同主族性质的递变规律是解题关键,注意钠与氧气反应条件不同产物不同.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.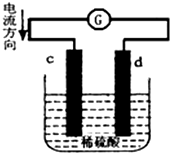 将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
 将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )
将锌片和铜片同时插入100mL 稀硫酸中,组成的原电池装置如图所示(c、d为两个电极,电池工作过程中溶液体积不变).下列有关判断不正确的是( )| A. | 当电路中通过2 mol 电子时,d 极可以生成22.4 L H2 | |
| B. | 当电路中通过0.1 mol 电子时,溶液中c(Zn2+)=0.5 mol•L-1 | |
| C. | c为负极,发生氧化反应 | |
| D. | 电池工作完成后,溶液中SO42-浓度基本不变 |
16.某研究小组为了探究“铁与水蒸气”的反应的产物,进行了下列实验:用如图1所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒高温下不与水和铁反应).

(1)如何检查该装置的气密性:将C处导气管末端浸入水槽中,加热A处圆底烧瓶,导管末端出现气泡,停止加热后导管末端出现一段水柱
(2)写出铁与水蒸气反应的化学方程式3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水.
在答题卡上按下表的格式写出实验步骤、预期现象与结论.
步骤1中加入足量1mol/L CuSO4溶液的作用是除去反应后固体中可能未反应完的铁粉,以免影响后续实验的结果分析.
(4)固体产物中铁元素的质量分数的测定可采用图2的流程.其中步骤①是向溶液中加入锌粉至黄色刚好消失;步骤②用0.010mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液平均为v mL.(已知5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O)其中加入锌粉的目的是将Fe3+还原为Fe2+.实验测得ag样品中固体产物铁元素的质量分数为$\frac{250×5×56g/mol×0.010mol/L×V×1{0}^{-3}L}{25a}$×100%_(只列计算表达式).

(1)如何检查该装置的气密性:将C处导气管末端浸入水槽中,加热A处圆底烧瓶,导管末端出现气泡,停止加热后导管末端出现一段水柱
(2)写出铁与水蒸气反应的化学方程式3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水.
在答题卡上按下表的格式写出实验步骤、预期现象与结论.
| 实验步骤 | 预期现象与结论 | |
| 步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的3mol/LH2SO4,振荡溶解,过滤后将滤液配成250mL溶液,待用. | - |
| 步骤2 | 取少量步骤1中滤液于试管中,滴加1~2滴20%KSCN | 溶液变红色,则固体产物含+3价铁 |
| 步骤3 | 取少量步骤1中滤液于试管中,滴加1~2滴0.01mol/LKMnO4 | 溶液紫色褪去,则固体产物含+2价铁 |
(4)固体产物中铁元素的质量分数的测定可采用图2的流程.其中步骤①是向溶液中加入锌粉至黄色刚好消失;步骤②用0.010mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液平均为v mL.(已知5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O)其中加入锌粉的目的是将Fe3+还原为Fe2+.实验测得ag样品中固体产物铁元素的质量分数为$\frac{250×5×56g/mol×0.010mol/L×V×1{0}^{-3}L}{25a}$×100%_(只列计算表达式).
13.下列说法正确的是( )
| A. | 氯化钠和盐酸溶于水都发生电离,克服粒子间作用力的类型相同 | |
| B. | 金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | |
| C. | HI的分子质量大于HF,所以HI的沸点高于HF | |
| D. | 由IA族和VIA族元素形成的原子个数比为l:1,离子个数比为2:l的化合物是含有共价键的离子化合物 |
20.关于下列各实验装置的叙述中,正确的是( )
| A. | 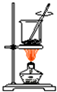 海带烧成灰 海带烧成灰 | |
| B. | 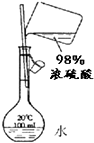 配制稀硫酸 配制稀硫酸 | |
| C. |  分离碘并回收苯 分离碘并回收苯 | |
| D. |  X为CCl4,可用于吸收HCl,并防止倒吸 X为CCl4,可用于吸收HCl,并防止倒吸 |
10.下列各组物质中,既不是同系物,又不是同分异构体的是( )
| A. | 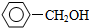 和 和 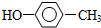 | B. | 苯甲酸和 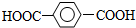 | ||
| C. | 乙酸和硬脂酸 | D. | 硝基乙烷和氨基乙酸 |
17.北京时间9月25日21时10分04秒,我国航天事业又迎来一个历史性时刻,我国自行研制的神舟七号载人飞船在酒泉卫星发射中心发射升空,于28日下午回到美丽的地球.“神舟”七号汇集了大量最新科技,发射火箭的常规推进剂为四氧化氮和偏二甲肼(C2H8N2),5.00g C2H8N2完全燃烧可放出212.5kJ热量.下列叙述正确的是( )
| A. | 燃烧不一定有氧气参加,也不一定是放热反应 | |
| B. | 火箭点火后,喷出的红色火焰是金属的焰色反应产生的 | |
| C. | 火箭燃料燃烧主要是将化学能转变为热能和光能,可能对环境产生污染 | |
| D. | 偏二甲肼燃烧的热化学方程式是:C2H8N2(g)+2N2O4(g)═2N2(g)+2CO2(g)+4H2O(g);△H=-2550kJ/mol |
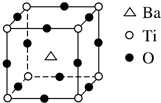 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题: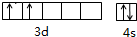 ;
;