��Ŀ����
����Ŀ����ѧ�ϳ���AG��ʾ��Һ�е����ȣ�AG��lg![]() ��25��ʱ����0.100 mol��L��1��NaOH��Һ�ζ�20��0 mL 0.100 mol��L��1ij�ᣨHA����Һ��AG������NaOH��Һ�������V����ϵ��ͼ��ʾ������˵����ȷ����
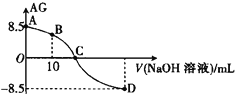
��25��ʱ����0.100 mol��L��1��NaOH��Һ�ζ�20��0 mL 0.100 mol��L��1ij�ᣨHA����Һ��AG������NaOH��Һ�������V����ϵ��ͼ��ʾ������˵����ȷ����
A. B����Һ�д���2c��H������2c��OH������c��A������c��HA��
B. C��ʱ������NaOH��Һ���������20��00 mL
C. �ζ�������Ӧ��ѡ�������ָʾ��
D. 25��ʱ������HA�ĵ���ƽ�ⳣ��Ka��1��0��10��5.5
���𰸡�A
��������
��ͼ��֪��A��lg![]() =8.5����Kw=1.0��10-14�ɵ�c2��H+��=1.0��10-5.5��c��H������0.100 mol��L��1����HAΪ���B��Ϊ��Ũ�ȵ�HA��NaA�����Һ����Һ�����ԣ�C��ʱc��H����=c��OH��������Һ�����ԣ�ΪHA��NaA�����Һ����HA��Һ��ȫ��Ӧʱ������NaOH��Һ�����Ϊ20��00 mL��
=8.5����Kw=1.0��10-14�ɵ�c2��H+��=1.0��10-5.5��c��H������0.100 mol��L��1����HAΪ���B��Ϊ��Ũ�ȵ�HA��NaA�����Һ����Һ�����ԣ�C��ʱc��H����=c��OH��������Һ�����ԣ�ΪHA��NaA�����Һ����HA��Һ��ȫ��Ӧʱ������NaOH��Һ�����Ϊ20��00 mL��
A���ͼ��֪��B��Ϊ��Ũ�ȵ�HA��NaA�����Һ����Һ�����ԣ���Һ�д��ڵ���غ��ϵc��H+��+c��Na+��=c��OH-��+c��A-���������غ��ϵ2c��Na+��=c��HA��+c��A-��������ʽ�ϲ��ɵ�2c��H+��-2c��OH-��=c��A-��-c��HA������A��ȷ��
B���ͼ��֪��C��ʱc��H����=c��OH��������Һ�����ԣ�ΪHA��NaA�����Һ��HAδ��ȫ��Ӧ�������NaOH��Һ�����С��20��00 mL����B������
C�ǿ�������ʱ����Ӧ����ǿ�������Σ������ȫ��Ӧʱ��Һ�Լ��ԣ�Ӧѡ���̪��ָʾ������C����
D���ͼ��֪��A��lg![]() =8.5����Kw=1.0��10-14�ɵ�c2��H+��=1.0��10-5.5��c��H����=
=8.5����Kw=1.0��10-14�ɵ�c2��H+��=1.0��10-5.5��c��H����=![]() ��HA�ĵ��볣��Ka=
��HA�ĵ��볣��Ka=![]() =
=![]() =1��10-4.5����D����
=1��10-4.5����D����
��ѡA��

 ��У����ϵ�д�
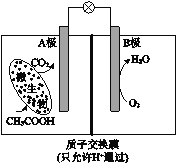
��У����ϵ�д�����Ŀ��CH4-CO2�������������Եõ��ϳ�����CO��H2����������������ļ��ž�����Ҫ���塣�ش��������⣺
��1��CH4-CO2��������ӦΪ��CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g)��
2CO(g)+2H2(g)��
��֪��C(s)+2H2(g) = CH4(g) ��H= -76 kJ��mol1
C(s)+O2(g) = CO2(g) ��H= -394 kJ��mol1
2C(s)+ O2(g) =2 CO(g) ��H= -222 kJ��mol1
�ô�������Ӧ����H=______kJ��mol1�����������CH4ƽ��ת���ʵ������ǣ����ţ���______________
A�����µ�ѹ B�����¸�ѹ C�����¸�ѹ D�����µ�ѹ
ij�¶��£������Ϊ2 L�������м���2 mol CH4��1 mol CO2�Լ���������������Ӧ���ﵽƽ��ʱCO2��ת������50%����ƽ�ⳣ��Ϊ___mol2��L2��
��2����Ӧ�д������Ի����̼��Ӧ�����ͣ�ͬʱ���ڵ���̼��Ӧ��ʹ��̼�����١�����������±���
��̼��Ӧ�� CH4(g) | ��̼��Ӧ�� CO2(g)+C(s) | ||
��H/(kJ��mol1) | +75 | +172 | |
���/ (kJ��mol1) | ����X | 33 | 91 |
����Y | 43 | 72 | |
���ϱ��жϣ�����X_______Y�������������������������������ǣ�____________��
�ڷ�Ӧ��������ɡ�ѹǿ����Ӧʱ����ͬ������£�ij��������Ļ�̼�����¶ȵ� �仯��ϵ��ͼ��ʾ�������¶�ʱ�����й��ڻ�̼��Ӧ����̼��Ӧ��ƽ�ⳣ��(K)������(��)��������ȷ����________���ţ���

A��K����K��������
B������������������
C��K������K������
D���������ӵı������������ӵı�����
����һ���¶��£����ij�����ϳ���̼���������ʷ���Ϊ��=k��p(CH4)��[p(CO2)]-0.5(kΪ���ʳ���)����p(CH4)һ��ʱ����ͬp(CO2)�»�̼����ʱ��ı仯������ͼ��ʾ����pa(CO2)��pb(CO2)��pc(CO2)�Ӵ�С��˳��Ϊ____��