��Ŀ����
����Ŀ���ձ���װ��50mLH2SO4�� Na2SO4 �Ļ��Һ����Ũ�ȷֱ�Ϊ 0.16mol/L �� 2mol/L����ʹ��Ũ�ȷֱ��Ϊ 1.6mol/L �� 0.2mol/L����ֻ������ˮ�� 18mol/L ŨH2SO4�Լ���Ҫ�����������£��������
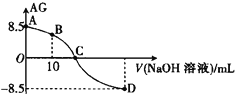
��1����ͼ��ʾ����������������Һ�����õ�����_____������ĸ�������ƹ����л�ȱ�ٵIJ���������_____�����������ƣ�

��2�����в�����������������ҺŨ��ƫ�ߵ���_____
A������ƿ��ԭ��������������ˮ
B������ʱ�����ӹ۲�̶���
C������Ͳϴ�� 2��3 �Σ�����ϴ��Һȫ��ת��������ƿ��
D��û��������ˮϴ�ձ� 2��3 �Σ�����ϴҺ��������ƿ��
��3��ʵ����������У�Ӧ��ȡ______mL18molL��1��Ũ H 2SO4��Һ.
���𰸡�C 500mL����ƿ BC 44
��������
�ձ���װ��50mLH2SO4�� Na2SO4 �Ļ��Һ����ʹ��Na2SO4Ũ����2mol/L��Ϊ0.2mol/L����Һ���Ӧ�ñ�Ϊ![]() =500mL��H2SO4��Ũ����0.16mol/L����Ϊ1.6mol/L�����Ũ��������ʵ�����0.5L��1.6mol/L��0.05L��0.16mol/L=0.792mol������Ҫ������������һ�������Ũ���ᣬ�ټ�������ˮϡ�͵�500mL��
=500mL��H2SO4��Ũ����0.16mol/L����Ϊ1.6mol/L�����Ũ��������ʵ�����0.5L��1.6mol/L��0.05L��0.16mol/L=0.792mol������Ҫ������������һ�������Ũ���ᣬ�ټ�������ˮϡ�͵�500mL��
��1��Ҫ������������һ�������Ũ���ᣬ�ټ�������ˮϡ�͵�500mL����Ҫ���������ձ�������������Ͳ��500 mL����ƿ����ͷ�ιܣ���ͼ��ʾ�������в����õ����Ƿ�Һ©����ѡC�����ƹ����л�ȱ�ٵIJ���������500 mL����ƿ��
��2��A������ƿ��ԭ��������������ˮ����������ҺŨ����Ӱ�죬�ʲ�ѡA��
B������ʱ�����ӹ۲�̶��ߣ���Һ���ƫС��������ҺŨ��ƫ�ߣ���ѡB��
C������Ͳϴ�� 2��3 �Σ�����ϴ��Һȫ��ת��������ƿ�У��������ʵ���ƫ�࣬������ҺŨ��ƫ�ߣ���ѡC��
D��û��������ˮϴ�ձ� 2��3 �Σ�����ϴҺ��������ƿ�У��������ʵ���ƫ�٣�������ҺŨ��ƫС���ʲ�ѡD��
��3�����Ũ��������ʵ�����0.5L��1.6mol/L��0.05L��0.16mol/L=0.792mol����Ũ����������![]() 0.044L=44 mL��ʵ����������У�Ӧ��ȡ44 mL18molL��1��Ũ H2SO4��Һ��
0.044L=44 mL��ʵ����������У�Ӧ��ȡ44 mL18molL��1��Ũ H2SO4��Һ��

����Ŀ��PbCO3���������ᡢ�մɺͲ����ȹ�ҵ���ɷ�Ǧ��(��Ҫ�ɷ�ΪPbS����������FeS��)�����̿�(��Ҫ�ɷ�ΪMnO2)�Ʊ�PbCO3���������£�

��֪��PbCl2��������ˮ���Ҵ�����������ˮ�������ʵ��ܶȻ����±����Իش��������⣺
���� | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | PbCl2 | PbS | PbCO3 |
Ksp | 2��10-13 | 8.0��10-16 | 1��10-38 | 1.6��10-5 | 8.0��10-28 | 7.4��10-14 |
(1)PbCO3��������________��
(2)�������MnO2��������________��������ͼ�����ٵ���ѷ�Ӧ������________��

(3)����ڳ��ȳ��˵�ԭ����___________________��
(4)�����ϴ���õ��Լ���____________��
(5)����ҺY���ữ��Ȼ�����MnO2����Ӧ�����ӷ���ʽΪ__________������Ӧ��c(Mn2+)=0.2mol/L����һ��������Һ��pH�ɷ���Fe3+��Mn2+����Һ������pH��ΧΪ_______[c(Fe3+)��1��10-5 mol/Lʱ��ʾFe3+�ѳ�����ȫ]��
(6)����ܷ�Ӧ�����ӷ���ʽΪ______________��
(7)��ƷPbCO3��������PbCl2���ʣ��ᴿ��ʵ�鷽����________��