题目内容
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl;
2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2FeCl2 + Cl2 = 2FeCl3
复分解反应: 2CH3COOH + K2CO3 = 2CH3COOK+ CO2 ↑ + H2O;
KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应: 4NaClO 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是
| A.还原性(酸性溶液):Fe2+> I- > Cl- |
| B.氧化性(酸性溶液):Co(OH)3 >Fe3+ > I2 |
| C.酸性(水溶液):CH3COOH >H2CO3 >HCN |
| D.热稳定性:NaCl>NaClO4>NaClO |
A
解析试题分析:A、在2FeCl3+2HI═2FeCl2+I2+2HC反应中,还原性:I—>Fe2+。在2FeCl2 + Cl2=2FeCl3反应中,还原性是Fe2+>Cl—,故还原性应为:I—>Fe2+>Cl—,故A错误;B、在2FeCl3+2HI═2FeCl2+I2+2HC反应中,氧化性:FeCl3>I2。在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2,又Cl2>FeCl3,故Co(OH)3>FeCl3,则有:Co(OH)3>FeCl3>I2,B正确;C、化学反应遵循强酸制弱酸的规律,在反应2CH3COOH + K2CO3=2CH3COOK+ CO2 ↑ + H2O中,酸性CH3COOH>H2CO3。在反应中KCN+CO2+H2O═HCN+KHCO3,酸性H2CO3>HCN,则酸性为CH3COOH>H2CO3>HCN,C正确;D、物质分解时生成更加稳定的物质,在反应中4NaClO 3NaCl+NaClO4,稳定性NaClO4>NaClO,在反应中NaClO4
3NaCl+NaClO4,稳定性NaClO4>NaClO,在反应中NaClO4 NaCl+2O2↑中,稳定性NaCl>NaClO4,则稳定性NaCl>NaClO4>NaClO,故D正确,答案选A。
NaCl+2O2↑中,稳定性NaCl>NaClO4,则稳定性NaCl>NaClO4>NaClO,故D正确,答案选A。
考点:考查氧化性、还原性、酸性以及物质热稳定性的比较

 阅读快车系列答案
阅读快车系列答案铜在潮湿的空气中会产生铜绿,其反应为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3。下列有关该反应的说法不正确的是( )
| A.该反应是化合反应 |
| B.该反应中氧气是氧化剂,单质铜是还原剂 |
| C.该反应是氧化还原反应,其中Cu得电子,O2失电子 |
| D.该反应是氧化还原反应,只有两种元素的化合价发生了变化 |
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O=7X+5FeSO4+12H2SO4,下列说法正确的是( )
| A.X的化学式为CuS,它既是氧化产物又是还原产物 |
| B.5molFeS2发生反应,有10mol电子转移 |
| C.产物中的SO42-离子有一部分是氧化产物 |
| D.FeS2只作还原剂 |
下列过程中不涉及氧化还原反应的是( )
| A.由植物油制备人造黄油 |
| B.用氯化铁溶液腐蚀印刷线路板 |
| C.用牺牲阳极的阴极保护法防止金属被腐蚀 |
| D.在蛋白质溶液中加入饱和硫酸铵溶液,析出白色固体 |
将几滴KSCN(SCN-是“类卤离子”)溶液加入到含有Fe3+的酸性溶液中,溶液变成红色。将该红色溶液分为两份:①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去。以下推测肯定不正确的是
| A.①中红色褪去的原因是KMnO4将SCN-氧化 |
| B.②中红色褪去的原因是SO2将Fe3+还原成Fe2+ |
| C.②中红色褪去的原因是SO2将SCN-还原 |
| D.SCN-在适当条件下可失去电子被氧化为(SCN)2 |
据报道,科学家发现了如下反应:O2+PtF6→O2(PtF6)。已知O2(PtF6)为离子化合物,其中Pt为+5价。对于此反应,下列说法正确的是
| A.此反应是非氧化还原反应 |
| B.O2(PtF6) 中氧元素的化合价是+1价 |
| C.在此反应中,O2是氧化剂,PtF6是还原剂 |
| D.此反应中,每生成1mol O2(PtF6)转移1mol 电子 |
钛被誉为“21世纪金属”。工业冶炼钛的第一步反应为:
TiO2+2C+2Cl2 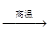 TiCl4+2CO。下列关于该反应的说法正确的是
TiCl4+2CO。下列关于该反应的说法正确的是
| A.TiO2是氧化剂 |
| B.氧化剂与还原剂的物质的量之比为1:1 |
| C.Cl2发生氧化反应 |
| D.当2 mol C参加反应时,转移的电子数目为2 mol |
下列物质的工业生产过程中,其主要反应不涉及氧化还原反应的是
| A.纯碱 | B.烧碱 | C.硫酸 | D.硝酸 |