题目内容
17.1~20号元素(稀有气体元素除外)中:(1)原子半径最小的是H,原子半径最大的是K.
(2)与水反应最剧烈的金属单质是K,非金属单质是F2.
(3)既能与酸反应,又能与碱反应的金属单质是Al.
(4)硬度最大的单质是C.
(5)气态氢化物的水溶液酸性最强的是Cl.
(6)最高价氧化物对应的水化物碱性最强的是K.
分析 (1)原子半径最小的为H,原子半径最大的为K;
(2)元素的金属性、非金属性越强,对应的单质越活泼,与水反应越剧烈;
(3)既能与酸反应,又能与碱反应的金属单质为Al;
(4)金刚石硬度最大;
(5)HCl溶液酸性最强;
(6)元素的非金属性越强,对应的最高价氧化物的水化物的碱性越强.
解答 解:(1)同周期元素从左到右,原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则-20号元素中原子半径最小的为H,原子半径最大的为K,
故答案为:H;K;
(2)同周期元素从左到右,金属性逐渐减弱,同主族元素从上到下,金属性逐渐增强,则金属性最强的为K,与水反应最剧烈,
非金属性最强的元素为F,F2与水剧烈反应,
故答案为:K;F2;
(3)既能与酸反应,又能与碱反应的金属单质为Al,故答案为:Al;
(4)金刚石硬度最大,为C的单质,故答案为:C;
(5)HCl溶液酸性最强,故答案为:Cl;
(6)1~20号元素中,K的金属性最强,对应的最高价氧化物对应的水化物碱性最强,故答案为:K.
点评 本题考查元素周期表、周期律知识,为高频考点,侧重于学生的分析能力的考查,注意把握元素的性质的递变规律,难度不大.

练习册系列答案
相关题目
8.下面是人们对于化学科学的各种常见的认识,其中错误的是( )
| A. | 化学将为环境、能源、资源等问题的解决提供有力保障 | |
| B. | 化学正发展成为一门实验与理论互相结合、互相渗透的科学 | |
| C. | 化学是一门具有极强实用性的自然科学 | |
| D. | 化学是一门纯实验的自然科学,实验是探究化学过程的唯一途径 |
5.关于下列图示装置运用的叙述正确的是( )
①装置甲可防止铁钉生锈
②装置乙可除去乙烷中混有的乙烯
③装置丙可验证HCl气体在水中的溶解性
④装置丁可除去乙酸乙酯中混有的乙酸
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体.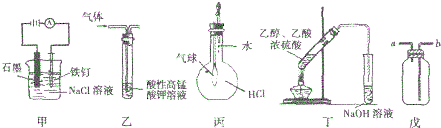
①装置甲可防止铁钉生锈
②装置乙可除去乙烷中混有的乙烯
③装置丙可验证HCl气体在水中的溶解性
④装置丁可除去乙酸乙酯中混有的乙酸
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体.

| A. | ③⑤ | B. | ③④ | C. | ①②④ | D. | ①③⑤ |
2.下表是元素周期表的一部分,针对表中的①~⑩中元素,用化学用语填空回答以下问题:
(1)在这些元素中,最活泼的非金属元素是F化学性质最不活泼元素原子的原子结构示意图为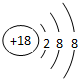 ;
;
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3;
(3)最强碱的电子式为: ①的气态氢化物的电子式:
①的气态氢化物的电子式: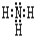 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 ;
;(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3;
(3)最强碱的电子式为:
 ①的气态氢化物的电子式:
①的气态氢化物的电子式: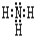 .
.
9.下列实验操作中正确的是( )
| A. | 用湿润的pH试纸测定某稀醋酸溶液的pH | |
| B. | 做完银镜反应的试管可以用氨水来洗涤 | |
| C. | 为了除去苯中混有的少量苯酚,加入足量浓溴水,充分搅拌后过滤分离 | |
| D. | 如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗 |
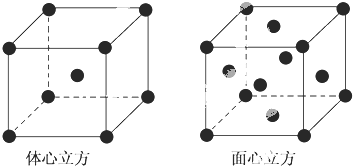
6.下列关于范德华力影响物质性质的叙述中,正确的是( )
| A. | 范德华力是决定由分子构成物质熔、沸点高低的惟一因素 | |
| B. | 范德华力与物质的性质没有必然的联系 | |
| C. | 范德华力能够影响物质的化学性质和物理性质 | |
| D. | 范德华力仅是影响物质部分物理性质的一种因素 |
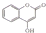 ,常用于制备抗凝血药,可通过下列流程合成:
,常用于制备抗凝血药,可通过下列流程合成:
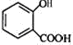 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$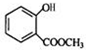 +H2O.
+H2O.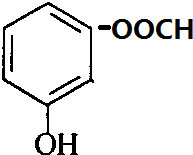 、
、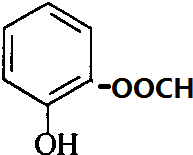 、
、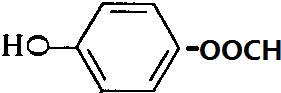 .
.
 ;(取代反应).
;(取代反应).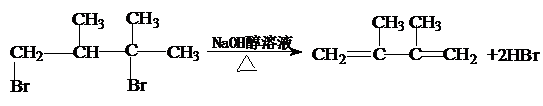 ; (消去反应).
; (消去反应).