题目内容
下列哪种说法可以证明反应.N2+3H2 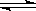 2NH3已达到平衡状态 ( )
2NH3已达到平衡状态 ( )
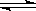 2NH3已达到平衡状态 ( )
2NH3已达到平衡状态 ( ) | A.1个N≡N键断裂的同时,有6个H—H键断裂 |
| B.1个N≡N键断裂的同时,有3个H—H键断裂 |
| C.1个N≡N键断裂的同时,有6个N—H键断裂 |
| D.1个N≡N键断裂的同时,有6个N—H键形成 |
C
试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。选项ABD中反应速率的方向是相同的,一定不能说明。C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,可以说明,答案选C。
点评:该题是中等难度的试题,该题也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和抽象思维能力。该题的关键是明确平衡状态的特点,如何结合具体的可逆反应灵活运用即可。

练习册系列答案
相关题目
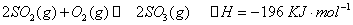 时,在2L固定容积的密闭容器中充入2mol
时,在2L固定容积的密闭容器中充入2mol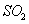 和2mol
和2mol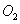 ,10分钟后达到平衡,
,10分钟后达到平衡,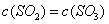
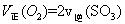 )
)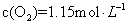 ,请在图上画出15-25分钟
,请在图上画出15-25分钟 的浓度变化曲线。
的浓度变化曲线。
 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( ) CO(g)+H2(g);
CO(g)+H2(g); CO2(g)+H2(g)
CO2(g)+H2(g) CH3OH(g)
CH3OH(g)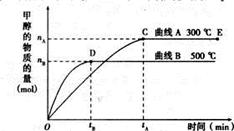
 2C(g)达平衡,设初始A、B的物质的量分别为Xmol、Ymol,若要使平衡时反应物总物质的量与生成物总物质的量相等,则X/Y应满足的是
2C(g)达平衡,设初始A、B的物质的量分别为Xmol、Ymol,若要使平衡时反应物总物质的量与生成物总物质的量相等,则X/Y应满足的是  2Z(g)达到限度的标志是
2Z(g)达到限度的标志是  C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是