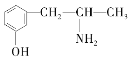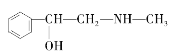题目内容
【题目】在恒容绝热密闭容器中发生CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g),下列情况都能说明该反应已达到平衡状态的是
2N2(g)+CO2(g)+2H2O(g),下列情况都能说明该反应已达到平衡状态的是
①容器内混合气体的平均相对分子质量不再变化;
②容器内气体分子个数不再发生变化;
③容器内气体的压强不再发生变化;
④v正(NO):v逆(N2):V逆(CO2)=4:2:1
A.①②③B.③④C.①②③④D.②③④
【答案】B
【解析】
①反应前后气体质量、物质的量都不变,所以混合气体的平均相对分子质量是恒量,容器内混合气体的平均相对分子质量不变,不一定平衡,不选①;
②反应前后气体物质的量不变,容器内气体分子个数是恒量,分子数不变,不一定平衡,不选②;
③反应前后气体物质的量不变,绝热容器内温度改变,容器内气体的压强是变量,容器内气体的压强不变,一定平衡,选③;
④正逆反应速率比等于系数比,v正(NO):v逆(N2):V逆(CO2)=4:2:1,一定达到平衡状态,选④;
故选B。

【题目】(1)通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和减去反应中形成新化学键的键能之和。下面列举了一些化学键的键能数据,供计算使用。
化学键 | Si—O | Si—Cl | H-H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
已知:1mol晶体硅含有2molSi-Si键。工业上可以通过下列反应制取高纯硅:SiCl4(g)+2H2(g)=Si(s)+4HCl(g),则该反应的反应热(ΔH)为______。
(2)碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
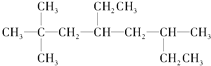
①有机物M经过太阳光光照可转化成N,转化过程如下:
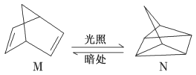 ΔH=+88.6 kJ·mol-1
ΔH=+88.6 kJ·mol-1
则M的化学式为_________________,M、N相比,较稳定的是____________。(填M或N)
②已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a____________238.6(填“>”、“<”或“=”)。
③使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________。
④火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,每转移1 mol电子时放出的热量为_______。
(3)已知:
①H2O(g)=H2O(l) △H1=—Q1kJ/mol
②CH3OH(g)=CH3OH(l) △H2=—Q2kJ/mol
③2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=—Q3kJ/mol(Q1、Q2、Q3均大于0)
若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为______kJ。