题目内容
下列反应的离子方程式正确的是( )
| A、碳酸钙与稀硝酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| C、铁溶于稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
| D、氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成硝酸钙、二氧化碳和水;
B.二者反应生成氢氧化钠和氢气;
C.二者反应生成NO和硝酸铁;
D.二者反应还生成水.
B.二者反应生成氢氧化钠和氢气;
C.二者反应生成NO和硝酸铁;
D.二者反应还生成水.
解答:
解:A.二者反应生成硝酸钙、二氧化碳和水,离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,故A正确;
B.二者反应生成氢氧化钠和氢气,离子方程式为2Na+2H2O═2Na++2OH-+H2↑,故B正确;
C.二者反应生成NO和硝酸铁,离子方程式为Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.二者反应还生成水,离子方程式为 Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故D错误;
故选AB.
B.二者反应生成氢氧化钠和氢气,离子方程式为2Na+2H2O═2Na++2OH-+H2↑,故B正确;
C.二者反应生成NO和硝酸铁,离子方程式为Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.二者反应还生成水,离子方程式为 Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故D错误;
故选AB.
点评:本题考查了离子方程式正误判断,根据物质的溶解性、离子方程式的书写规则来分析解答,注意C中不能生成氢气,因为硝酸具有强氧化性,为易错点.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
下列图象与对应的说法正确的是( )
A、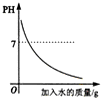 向NaOH溶液中加水稀释 |
B、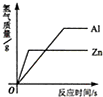 等质量的Al、Zn与足量的稀硫酸反应 |
C、 向稀硫酸中加入Ba(OH)2溶液 |
D、 恒温下,适量蒸发饱和NaCl溶液的水分 |
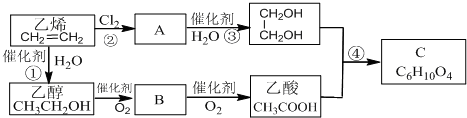
下列关于乙烯的用途的说法不正确的是( )
| A、制塑料 |
| B、生产有机溶剂 |
| C、常作气体燃料 |
| D、作果实催熟剂 |
 常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )
常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )| A、点①所示溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | ||
| B、点②所示溶液中:c(CH3COOH)>c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | ||
| C、点③所示溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | ||
D、在整个滴定过程中:溶液中
|
甲、乙、丙、丁四种短周期主族元素,它们的价电子数依次增大,乙形成的化合物种类最多,甲与乙的原子序数之和等于丁的原子序数,丙和乙位于同一周期,丁和乙位于不同周期.则下列说法中正确的是( )
| A、甲、乙、丙形成的化合物既有离子键又有共价键 |
| B、乙、丙、丁形成的氢化物常温下均为气体 |
| C、原子序数由小到大顺序为:甲<乙<丙<丁 |
| D、原子半径大小顺序为:丁>甲>乙>丙 |
下列叙述不正确的是( )
| A、金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B、在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C、在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
下列离子方程式正确的是( )
| A、SiO2与NaOH溶液:SiO2+2Na++2OH-═Na2SiO3↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C、向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |