题目内容
某软质隐形眼镜材料为如图所示的聚合物.下列有关说法错误的是( )
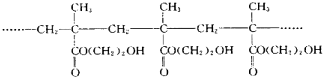

| A、生成该聚合物的反应属于加聚反应 |
| B、该聚合物的单体是丙酸乙酯 |
| C、该聚合物分子中存在大量的-OH,所以具有较好的亲水性 |
D、该聚合物的结构筒式为: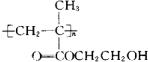 |
考点:有机高分子化合物的结构和性质
专题:有机物的化学性质及推断
分析:A.甲基丙烯酸羟乙酯发生加聚反应,生成高分子化合物聚甲基丙烯酸羟乙酯;
B.丙酸乙酯无碳碳双键,不能加聚;
C.易与水结合的基团称为亲水基团(如-NH2、-COOH、-OH);
D.根据图示高聚物判断;
B.丙酸乙酯无碳碳双键,不能加聚;
C.易与水结合的基团称为亲水基团(如-NH2、-COOH、-OH);
D.根据图示高聚物判断;
解答:
解:A.生成该聚合物,加聚反应为nCH2=C(CH3)COOCH2CH2OH
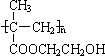 ,该反应是甲基丙烯酸羟乙酯通过加聚反应生成了高分子化合物的反应,故A正确;
,该反应是甲基丙烯酸羟乙酯通过加聚反应生成了高分子化合物的反应,故A正确;
B.该聚合物的单体是甲基丙烯酸羟乙酯,故B错误;
C.该聚合物分子中存在大量的-OH,和水能形成氢键,所以具有较好的亲水性,故C正确;
D.根据图示可知,该高聚物为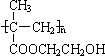 ,故D正确;
,故D正确;
故选B.
| 催化剂 |
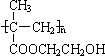 ,该反应是甲基丙烯酸羟乙酯通过加聚反应生成了高分子化合物的反应,故A正确;
,该反应是甲基丙烯酸羟乙酯通过加聚反应生成了高分子化合物的反应,故A正确;B.该聚合物的单体是甲基丙烯酸羟乙酯,故B错误;
C.该聚合物分子中存在大量的-OH,和水能形成氢键,所以具有较好的亲水性,故C正确;
D.根据图示可知,该高聚物为
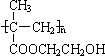 ,故D正确;
,故D正确;故选B.
点评:本题考查有机物的结构与性质,为高频考点,把握高聚物及其单体的性质为解答的关键,该题侧重烯烃、羧酸、醇、酯性质的考查,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
取a g某铁的氧化物R溶于足量稀盐酸,加水稀释至200mL,取20mL所得溶液,向其中滴加新制氯水,将其中的铁元素全部氧化为Fe3+,再向溶液中加入NaOH溶液使其完全沉淀,所得沉淀经过滤、洗涤,并将沉淀灼烧至质量不再变化,称量得b g固体,则( )
| A、若a:b=10:3,则R的化学式为Fe2O3 | ||
| B、若a:b=29:3,则R的化学式为Fe3O4 | ||
| C、若a:b=9:32,则R的化学式为FeO | ||
D、实验过程中被还原的Cl2为
|
下列有关溶液中离子浓度的关系,不正确的是( )
| A、NaHC03溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B、常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C、0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D、相同温度下,0.2mol/L的CH3COOH溶液中c(H+)小于0.1mol/L的CH3COOH中c(H+)的两倍 |
关于下列电解质溶液的说法中,正确的是( )
| A、常温下,10mL 0.2mol/L NH4NO3溶液与10mL 0.1mol/L NaOH溶液混合后所得pH=9.6的溶液中:c(NO3-)>c(NH4+)>c(Na+)>c(NH3?H2O)>c(OH-)>c(H+) |
| B、0.1mol/L Na2S溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C、常温下a mL 0.1mol/L KOH与b mL 0.1mol/L HCN两溶液混合后pH>7,则一定有a≥b |
| D、10mL 0.1mol/L NaCl溶液中离子总数为x,10mL 0.1mol/L CH3COONa溶液中离子总数为y,则x=y |
金属M和N可构成如图所示的装置.下列分析正确的是( )
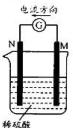

| A、金属活性性N>M |
| B、M逐渐溶解 |
| C、负极反应为2H++2e-═H2↑ |
| D、SO42-向M极定向移动 |