题目内容
某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法错误的是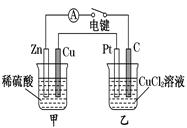
| A.甲装置是原电池,乙装置是电解池 |
| B.当甲中产生0.1 mol气体时,乙中析出固体的质量为6.4 g |
| C.实验一段时间后,甲烧杯中溶液的pH增大 |
| D.将乙中的C电极换成铜电极,则乙装置可变成电镀装置 |
D
解析试题分析:A、锌与稀硫酸反应生成硫酸锌与氢气,属于自发的氧化还原反应,即甲装置是原电池,其中锌是负极,铜是正极。乙装置是电解池,其中碳棒是阴极,Pt电极是阳极,A正确;B、甲中产生的气体是氢气,0.1mol氢气转移0.2mol电子,则依据电子守恒可知乙装置中析出铜的物质的量是0.1mol,质量是6.4g,B正确;C、甲装置中氢离子放电,溶液的酸性降低,因此实验一段时间后,甲烧杯中溶液的pH增大,C正确;D、乙装置中碳棒是阴极,因此将乙中的C电极换成铜电极,乙装置不能变成电镀装置,因为电镀装置中镀层金属应该作阳极,D不正确,答案选D。
考点:考查电化学原理的有关应用与判断

在下列装置中,MSO4和NSO4是两种常见金属的易溶盐。当K闭合时,SO42-从右到左通过交换膜移向M极,下列分析正确的是( )
| A.溶液中c(M2+)减小 |
| B.N的电极反应式:N-2e-=N2+ |
| C.X电极上有H2产生,发生还原反应 |
| D.反应过程中Y电极周围生成白色胶状沉淀 |
pH=a某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH<a,则该电解质可能是
| A.Ba(OH)2 | B.HCl | C.Na2SO4 | D.AgNO3 |
把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水配制成100 mL混合溶液,用石墨作电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下的体积相同。则下列描述正确的是( )
| A.电路中共转移0.9 mol电子 |
| B.阳极得到的气体中有O2,且其物质的量为0.35 mol |
| C.阴极的质量增加3.2 g |
| D.铝元素仅以Al(OH)3的形式存在 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )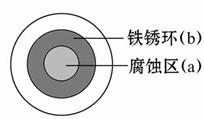
| A.液滴中的Cl-由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+ |
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+ Fe2++Cr3+。下列说法一定正确的是( )
Fe2++Cr3+。下列说法一定正确的是( )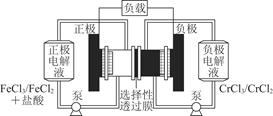
| A.充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B.电池放电时,负极的电极反应式为Fe2+-e-=Fe3+ |
| C.电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
| D.放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1 |
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体。Fe(OH)3有吸附性,可吸附污物使之沉积下来,具有净化水的作用。模拟处理装置如图所示,下列说法错误的是( )
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O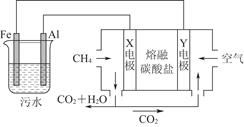 |
| B.铁作阳极,失去电子生成Fe2+ |
| C.工作时熔融盐中的碳酸根移向Y电极 |
| D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
| A.电池放电时,Na+从b极区移向a极区 |
| B.电极a采用MnO2,放电时它被还原 |
| C.该电池负极的电极反应式为BH4-+8OH--8e-=BO2-+6H2O |
| D.放电时,a极区溶液的pH升高,b极区溶液pH降低 |
