题目内容
【题目】有机合成是制药工业中的重要手段。G是某抗炎症药物的中间体,其合成路线如图:

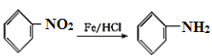
已知:
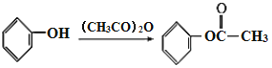 ,
,
(1)B的结构简式为_____。
(2)反应④的条件为____;①的反应类型为___;反应②的作用是____。
(3)下列对有机物G的性质推测正确的是____(填选项字母)。
A.具有两性,既能与酸反应也能与碱反应
B.能发生消去反应、取代反应和氧化反应
C.能聚合成高分子化合物
D.1mol G与足量NaHCO3溶液反应放出2mol CO2
(4)D与足量的NaOH溶液反应的化学方程式为_____。
(5)符合下列条件的C的同分异构体有___种。
A.属于芳香族化合物,且含有两个甲基 B.能发生银镜反应 C.与FeCl3溶液发生显色反应
其中核磁共振氢谱有4组峰,且峰面积之比为6∶2∶1∶1的是___(写出其中一种的结构简式)。
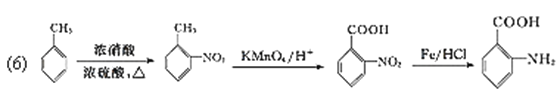
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的取代基连在苯环的间位。根据题中的信息,写出以甲苯为原料合成有机物![]() 的流程图(无机试剂任选)。_______
的流程图(无机试剂任选)。_______
合成路线流程图示例如图:X![]() Y
Y![]() Z…目标产物
Z…目标产物
【答案】![]() 浓硫酸、浓硝酸、加热 取代反应 保护酚羟基,以防被氧化 AC
浓硫酸、浓硝酸、加热 取代反应 保护酚羟基,以防被氧化 AC 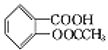 +3NaOH
+3NaOH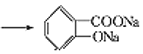 +CH3COONa+2H2O 16
+CH3COONa+2H2O 16 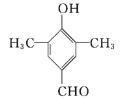 或
或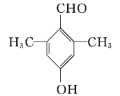
【解析】
根据D的结构简式(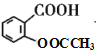 ),可知C分子中含有苯环,苯环上有两个邻位取代基,其中一个为-OOCCH3,另一个为烃基,被酸性高锰酸钾氧化为羧基生成D,B分子中有苯环,结合已知的第一个反应:
),可知C分子中含有苯环,苯环上有两个邻位取代基,其中一个为-OOCCH3,另一个为烃基,被酸性高锰酸钾氧化为羧基生成D,B分子中有苯环,结合已知的第一个反应: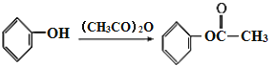 ,可知B分子中也有在苯环上处于邻位的两个取代基,其中一个是羟基,另一个是甲基,所以A是乙酸酐,由乙酰氯和乙酸发生取代反应生成。D在NaOH溶液中水解然后再酸化,得到的E为
,可知B分子中也有在苯环上处于邻位的两个取代基,其中一个是羟基,另一个是甲基,所以A是乙酸酐,由乙酰氯和乙酸发生取代反应生成。D在NaOH溶液中水解然后再酸化,得到的E为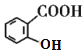 ,比较E和G的结构,再结合已知:
,比较E和G的结构,再结合已知: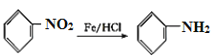 可知,E到F是发生了硝化反应,E中苯环羟基的对位碳原子上的氢原子被硝基取代生成了F,F到G是硝基被还原为氨基。
可知,E到F是发生了硝化反应,E中苯环羟基的对位碳原子上的氢原子被硝基取代生成了F,F到G是硝基被还原为氨基。
(1)从上面的分析可知,B的结构简式为![]() ;
;
(2)反应④是硝化反应,需要浓硝酸作反应物,浓硫酸作催化剂,而且反应还需加热;①是取代反应,反应②的作用是保护酚羟基,以防被高锰酸钾氧化。故答案为:浓硫酸、浓硝酸、加热;取代反应;保护酚羟基,以防被氧化;
(3)G的结构简式为 ;
;
A.G中有羧基,显酸性,还有氨基,显碱性,所以G具有两性,既能与酸反应也能与碱反应,故A正确;
B.醇可以发生消去反应,但酚不能发生消去反应,酚和羧酸都可以发生取代反应,酚羟基有还原性,可以被氧化,发生氧化反应,故B错误;
C.在G的分子中既有羧基,又有羟基,可以发生缩聚反应,生成聚酯,故C正确;
D.能和NaHCO3溶液反应放出CO2的只能是羧基,而1mol羧基只能生成1mol CO2,故1molG与足量NaHCO3溶液反应放出1molCO2,故D错误;
故选AC;
(4)D的结构简式为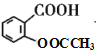 ,与足量的NaOH溶液反应时,羧基可以和NaOH发生酸碱中和,酯基可以发生水解,水解后生成的不是醇,而是酚,会继续和NaOH发生中和反应,所以1mol D能消耗3mol NaOH,发生反应的化学方程式为
,与足量的NaOH溶液反应时,羧基可以和NaOH发生酸碱中和,酯基可以发生水解,水解后生成的不是醇,而是酚,会继续和NaOH发生中和反应,所以1mol D能消耗3mol NaOH,发生反应的化学方程式为 +3NaOH
+3NaOH +CH3COONa+2H2O;
+CH3COONa+2H2O;
(5)C为![]() ,C的同分异构体属于芳香族化合物,即含有苯环,与FeCl3溶液发生显色反应,苯环上直接连有羟基;能发生银镜反应,要求分子中有醛基。C的苯环上共有3个碳原子和2个氧原子,酚羟基和醛基各用了1个氧原子,醛基还用了1个碳原子,还有2个碳原子,根据含有两个甲基的要求,苯环上共有4个取代基,两个甲基,一个酚羟基和一个醛基;可以先固定两个甲基的位置,有邻、间、对三种位置,然后再连上酚羟基和醛基。当2个甲基处于邻位时,酚羟基和醛基有6种不同的位置,当2个甲基处于间位时,酚羟基和醛基有7种不同的位置,当2个甲基处于对位时,酚羟基和醛基有3种不同的位置,所以共有16种同分异构体。其中核磁共振氢谱有/span>4组峰,且峰面积之比为6∶2∶1∶1的是
,C的同分异构体属于芳香族化合物,即含有苯环,与FeCl3溶液发生显色反应,苯环上直接连有羟基;能发生银镜反应,要求分子中有醛基。C的苯环上共有3个碳原子和2个氧原子,酚羟基和醛基各用了1个氧原子,醛基还用了1个碳原子,还有2个碳原子,根据含有两个甲基的要求,苯环上共有4个取代基,两个甲基,一个酚羟基和一个醛基;可以先固定两个甲基的位置,有邻、间、对三种位置,然后再连上酚羟基和醛基。当2个甲基处于邻位时,酚羟基和醛基有6种不同的位置,当2个甲基处于间位时,酚羟基和醛基有7种不同的位置,当2个甲基处于对位时,酚羟基和醛基有3种不同的位置,所以共有16种同分异构体。其中核磁共振氢谱有/span>4组峰,且峰面积之比为6∶2∶1∶1的是 或
或 。故答案为16,
。故答案为16, 或
或 ;
;
(6)以甲苯为原料合成![]() ,需要在苯环上连上羧基和氨基,羧基可以通过甲基被氧化得到,氨基可以先在苯环上连上硝基,然后再还原得到。因为苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的取代基连在苯环的间位。最终合成的有机物
,需要在苯环上连上羧基和氨基,羧基可以通过甲基被氧化得到,氨基可以先在苯环上连上硝基,然后再还原得到。因为苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的取代基连在苯环的间位。最终合成的有机物![]() 的两个取代基在邻位,所以甲苯应先硝化,在甲基的邻位引入硝基,然后再氧化甲基成为羧基,最后还原硝基为氨基;流程为:
的两个取代基在邻位,所以甲苯应先硝化,在甲基的邻位引入硝基,然后再氧化甲基成为羧基,最后还原硝基为氨基;流程为: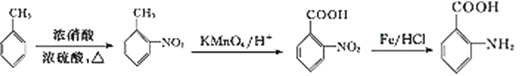 。
。

【题目】A和B两种有机物可以互溶,有关性质如下:
物质 | 密度(g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
A | 0.7893 | -117.3 | 78.5 | 与水以任意比混溶 |
B | 0.7137 | -116.6 | 34.5 | 不溶于水 |
(1)要除去A和B的混合物中的少量B,可采用的_______________方法可得到A。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
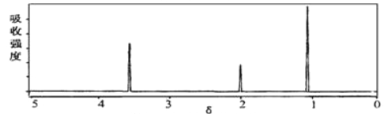
(2)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应且消耗6.72L(标准状况)氧气,生成5.4gH2O和8.8gCO2,则该物质的实验式是__________;质谱图显示,A的相对分子质量为46,又已知有机物A的核磁共振氢谱如图所示,则A的结构简式为________________。
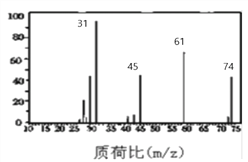
(3)下图是B的质谱图,则其相对分子质量为 ________ ,
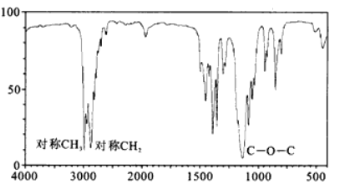
(4)B的红外光谱如图所示,则B的结构简式为__________________________。
(5)准确称取一定质量的A和B的混合物,在足量氧气充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增加14.4g和26.4g。计算混合物中A和B的物质的量之比_____________________。
【题目】硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)![]() 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度 | 450 | 500 | 550 | 600 |
SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(1)由表中数据判断△H________0(填“>”、“=”或“<”)。
(2)能判断该反应是否达到平衡状态的是___________。
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D. C(SO2)=C(SO3)
E.V正(SO2)=V正(SO3) F. V正(SO3)=2V逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1。
①0-2min之间,O2的反应速率为____。
②此时的温度为____℃。
③此温度下的平衡常数为_____(可用分数表示)。
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将_________向移动。