题目内容
15.下列各组混合物中,能用分液漏斗进行分离的是( )| A. | 水和四氯化碳 | B. | 碘和四氯化碳 | C. | 酒精和水 | D. | 汽油和植物油 |
分析 能用分液漏斗分离的物质,应为互不相溶的液体,以此解答.
解答 解:A.水和四氯化碳互不相溶,可用分液的方法分离,故A正确;
B.碘和四氯化碳互溶,不能用分液的方法分离,故B错误;
C.酒精和水互溶,不能用分液的方法分离,故C错误;
D.汽油和植物油互溶,不能用分液的方法分离,故D错误.
故选A.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质的异同,为解答该题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列说法中正确的是( )
| A. | H2O2的电子式: | |
| B. | ${\;}_{17}^{35}$Cl- 与${\;}_{17}^{37}$Cl属同位素 | |
| C. | 单质气体分子中不一定都具有共价键 | |
| D. | CaCl2晶体中既含有离子键又含有共价键 |
10.下列有关实验误差分析中,错误的是( )
| A. | 中和滴定实验中,盛装待测液的锥形瓶没有润洗,对实验结果无影响 | |
| B. | 用容量瓶配制一定物质的量浓度的溶液,定容时俯视刻度线,所配溶液浓度偏低 | |
| C. | 用润湿的pH试纸测某溶液的pH,测定结果不一定有误差 | |
| D. | 测定中和热的实验中,将碱液缓慢倒入酸溶液中,所测中和热值偏低 |
7.如图表示单质a与单质b在一定条件下反应生成c,其中c可能是( )
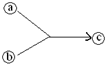

| A. | CuS | B. | FeS | C. | NO2 | D. | FeCl2 |
4.下列有机物命名正确的是( )
| A. | 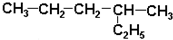 2-乙基戊烷 2-乙基戊烷 | B. | 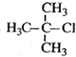 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | ||
| C. | 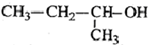 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
5.一定温度下反应2SO2(g)+O2(g)?2SO3(g)达到化学平衡状态的标志是( )
| A. | SO2,O2和SO3的体积分数不再改变 | |
| B. | c(SO2):c(O2):c(SO3)=2:1:2 | |
| C. | SO2与O2的物质的量之和是SO3的物质的量2倍 | |
| D. | 单位时间里每增加2molSO2,同时增加1molO2 |
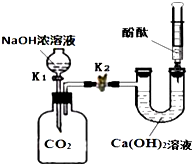 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.