题目内容
16.实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④用10%的NaOH溶液洗.正确的操作顺序是( )| A. | ①②③④ | B. | ④②③① | C. | ②④③① | D. | ④①②③ |
分析 根据粗苯中的成分及各试剂的作用分析,可溶性的物质易溶于水,所以用水洗涤易溶于水的物质;溴和氢氧化钠能反应所以可用氢氧化钠除去溴;干燥剂能吸收水分,利用物质沸点的不同可分离沸点不同的物质,据此分析.
解答 解:该反应中,铁和溴能反应生成溴化铁,溴化铁作催化剂且易溶于水,所以混合物中含溴化铁;苯和溴不可能完全反应,混合物中含有溴和苯;制取溴苯的同时还有溴化氢生成,所以混合物的成分有:溴化铁、溴、苯、溴苯、溴化氢.
所以操作顺序如下:a、HBr、溴化铁易溶于水而其它物质不易溶于水,所以先水洗洗去氢溴酸和溴化铁;
b、溴和氢氧化钠反应,所以用氢氧化钠洗去溴单质,残留部分氢氧化钠,氢氧化钠能溶于水而其他物质不溶于水,所以用水洗去多余的氢氧化钠;
c、用水洗涤后会残留部分水分,所以用干燥剂除去多余的水;
d、两者沸点不同,苯的沸点小,被蒸馏出,溴苯留在母液中,所以采取蒸馏的方法分离溴苯与苯.
故选C.
点评 本题考查了提纯粗溴苯的操作顺序,难度较大,首先要明确混合物中的成分,然后根据各物质的性质采取相应的方法去除杂质.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
6.欲除去CO2中的少量SO2,可选用( )
| A. | 饱和Na2CO3溶液 | B. | 饱和NaHCO3溶液 | C. | NaOH | D. | Ca(OH)2 |
1.分子式为C3H6Cl2的有机物,若再有一个氢原子被氯原子取代,生成的C3H5Cl3有两种同分异构体,原有的C3H6Cl2应该是( )
| A. | 1,3-二氯丙烷 | B. | 1,1-二氯丙烷 | C. | 1,2-二氯丙烷 | D. | 2,2-二氯丙烷 |
8.在密闭体积不变的真空容器中加入一定量纯净的氨基甲酸铵固体,(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10-3mol•L-1,下列说法中正确的是( )
| A. | 密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 | |
| B. | 20℃时,氨基甲酸铵的分解平衡常数为2.048×10-9mol3•L-3 | |
| C. | 恒温下压缩体积,NH3的体积分数不变 | |
| D. | 再加入一定量氨基甲酸铵,可加快正反应反应速率 |
5.燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量丙烯所产生的CO2的质量,该混合气体是( )
| A. | 丙烷、丁烯 | B. | 乙炔、丙烷 | C. | 乙烷、乙烯 | D. | 乙炔、乙烯 |
6.下表是元素周期律的一部分.根据表中的10种元素,用元素符号或化学式填空.
(1)在 ①~⑩元素中金属性最强的金属元素是K;第一电离能最小的元素是K;电负性最强的元素是F
(2)在 ①~⑩元素的最高价氧化物的水化物呈两性的是Al(OH)3;⑥形成的最高价氧化物的水化物的分子式是HClO4;
(3)①形成的气态氢化物的结构式是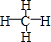 ;其中心原子采取sp3杂化,空间构型为正四面体.
;其中心原子采取sp3杂化,空间构型为正四面体.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑧ | ⑨ | ⑩ |
(2)在 ①~⑩元素的最高价氧化物的水化物呈两性的是Al(OH)3;⑥形成的最高价氧化物的水化物的分子式是HClO4;
(3)①形成的气态氢化物的结构式是
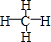 ;其中心原子采取sp3杂化,空间构型为正四面体.
;其中心原子采取sp3杂化,空间构型为正四面体. 
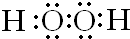 ,C元素在周期表中的位置是第二周期、第ⅦA族.
,C元素在周期表中的位置是第二周期、第ⅦA族.