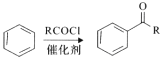
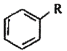
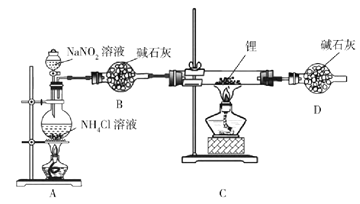
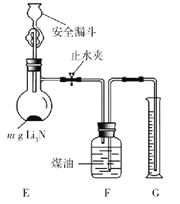
��Ŀ����
����Ŀ��ij��ѧС���ͬѧȡһ������Al��Fe2O3�Ļ����������ȷ�Ӧ����̽��������ijɷ֡���֪��Al��Fe���ۡ��е��������¡�
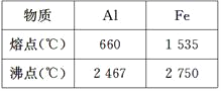
��ش��������⣺
��1��ijͬѧ�²⣬���ȷ�Ӧ���õ����������������Ͻ����ɣ��÷�Ӧ������ʹ���ۻ����������۵�����ͣ��������������γɺϽ�����Ϊ���Ľ����Ƿ������__(ѡ����������������������)�����һ����ʵ�鷽����֤���������õ��������к��н�������__��
��2������һ��ͬѧ�۲쵽������ʺ�ɫ������Ϊ���ȷ�Ӧ��������Fe3O4���ɣ���ͬѧ�������ʵ����֤���Ľ��ۣ�ȡ�����������ϡ�����ܽ⣬��ˮϡ�ͺ�μ�3��4��KSCN��Һ������Һ��Ϊ��ɫ������Fe3O4���ɣ�����û��Fe3O4���ɡ���ͬѧ��ʵ�鷽���Ƿ������____˵���������____��
���𰸡����� ȡ������Ʒ�����Թܣ�����NaOH��Һ���������ݲ�����˵���������������� ������ Fe3���������Ա�H��ǿ������������������Һ������Fe3����Ӧ��������Һ�в���Fe3����ͨ����ʵ�鲻��ȷ�����������Ƿ���Fe3O4
��������
(1)�������������۷е��жϣ���������������������Һ��Ӧ�ų��������м��飻
(2)���������ὫFe3����ԭΪFe2����
(1)�ӱ����е����ݿ�֪�����ȷ�Ӧ�ų��������ۻ�����ͬʱ��������Ҳ�ۻ����ʿɵõ������Ͻ���������������Һ��Ӧ��������������������Һ��Ӧ������������������Һ����������Ӧ��������������Ĵ��ڣ�ʵ�鷽���ǣ�ȡ������Ʒ�����Թܣ�����NaOH��Һ���������ݲ�����˵������������������
(2) Fe3���������Ա�H��ǿ������������������Һ������Fe3����Ӧ��������Һ�в���Fe3����ͨ����ʵ�鲻��ȷ�����������Ƿ���Fe3O4��

 һ����������ϵ�д�
һ����������ϵ�д�����Ŀ����¯������ұ��������Ҫ��������������Ҫ��ӦΪ��
Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g) ��H
2Fe(s)+3CO2(g) ��H
��Ӧ1�� Fe2O3(s)+3C(ʯī��s) ![]() 2Fe(s)+3CO(g) ��H1
2Fe(s)+3CO(g) ��H1
��Ӧ2�� C(ʯī��s)+CO2(g)![]() 2CO(g) ��H2
2CO(g) ��H2
�١�H= _________(�ú���H1�� ��H2����ʽ��ʾ��
�ڱ����¶Ȳ��䣬�ں��������н��з�Ӧ1���ﵽƽ��״̬���ٴγ���һ������CO (Fe����������ƽ��_________�ƶ�(������������ﵽ��ƽ���c(CO)��_________(��������С�����䡱)
(2)��T��ʱ����Ӧ Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g)��ƽ�ⳣ��K=64,��2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
2Fe(s)+3CO2(g)��ƽ�ⳣ��K=64,��2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
Fe2O3 | CO | Fe | CO2 | |
��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
��/mol | 1.0 | 1.5 | 1.0 | 1.0 |
�ټ�������CO��ƽ��ת����Ϊ_________
������˵����ȷ����_________������ĸ����
A��������ѹǿ�㶨��˵����Ӧ�ﵽƽ��״̬
B������Fe2O3���������CO��ת����
C����������CO��ƽ��ת���ʴ����ҵ�ƽ��ת����
D���������й����������ٸı䣬˵����Ӧ�ﵽƽ��״̬
��ȡ��ȷ�CO���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У���װ������Fe2O3������Ӧ��ͬʱ��ֱ�ⶨ��ϵ��CO�����������CO%�������������淴Ӧ�¶ȣ�T���仯�Ĺ�ϵͼ�����ڴ��������ƽ��ʱ��������ƽ����Է��������淴Ӧ�¶ȣ�T���ı仯ʾ��ͼ��
_________

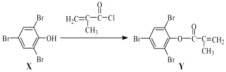
����Ŀ����ϩ(C3H6)����Ҫ���л�����ԭ�ϡ�����ֱ�������Ʊ�ϩ�����ķ�Ӧ�У�
��Ӧ����C3H8(g)C3H6(g)+H2(g) ��H1
��Ӧ����2C3H8(g)3C2H4(g)+2H2(g) ��H2
��֪������Ӧ�����Ea(��)С�ڷ�Ӧ�����Ea(��)��
��3�����ʵ�ȼ�������±���
C3H8(g) | C3H6(g) | H2(g) |
��2217.8kJ��mol-1 | ��2058kJ��mol-1 | ��285.8kJ��mol-1 |
��1����H1=_______kJ��mol-1
��2�����º��������£����ܱ������г���1molC3H8(g)�����������˵�����������Ʊ�ϩ��Ӧ�ﵽƽ��״̬����______________��
A���÷�Ӧ��H���ֲ���B����������ƽ��Ħ���������ֲ���
C��![]() ���ֲ���D��C3H8�ֽ�������C3H6�����������
���ֲ���D��C3H8�ֽ�������C3H6�����������
��3��һ���¶��£�������ܱ������г��������ʵ���Ϊ4mol�ı��������������壨�����������ǻ����������Ӧ��ͬʱ�䣬��ϩ������������Ĺ�ϵ��ͼ1��ʾ��ͼ���������ߵ�ԭ����______________��
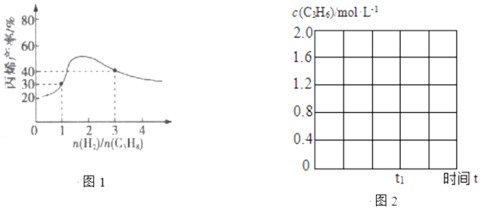
��4������Ӧ�¶�600������10molC3H8(g)����2L�ĸ��������У�����ƽ��ת�������ϩ��ѡ���Ծ�Ϊ40%����Ӧ����ƽ�ⳣ��K=______________��������2λС��������ϩ��ѡ����=![]() ��100%��
��100%��
��600�����������ⷴӦ��t1ʱ��ƽ�⣬����ͼ2�л�����������c(C3H6)��ʱ��t�ı仯ͼ��______________
��5����һ�ȱ���(C3H7Cl)�ķ�ˮ��ͨ���������������ƣ���Ƴ������س�ȥ����ԭ����ͼ3��ʾ��д��N�缫�ĵ缫��Ӧʽ______________��

����Ŀ����ҵ�ϳɰ����Ʊ�����һ��������������������£�
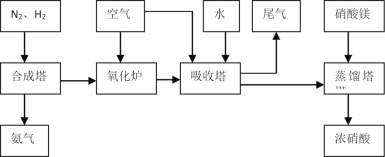
��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO(g)+H2O(g)![]() CO2(g)+H2(g)��
CO2(g)+H2(g)��
��t��ʱ����1L�ܱ������г���0.2molCO��0.3molˮ��������Ӧ����ƽ�����ϵ��c(H2)=0.12mol��L��1�����¶��´˷�Ӧ��ƽ�ⳣ��K=___��
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO������Ӧ���½���ƽ��ʱ��ˮ��������ת������(H2O)=___��
��2���ϳ����з�����ӦΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1___573K���>������<����=������
2NH3(g) ��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1___573K���>������<����=������
T/K | T1 | 573 | T2 |
K | 1.00��107 | 2.45��105 | 1.88��103 |
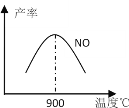
��3��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��4NH3+5O2![]() 4NO+6H2O ��H=��905kJ��mol��1 ����ͬ�¶���NO������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½��Ŀ���ԭ��___��
4NO+6H2O ��H=��905kJ��mol��1 ����ͬ�¶���NO������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½��Ŀ���ԭ��___��
��4���������з�ӦΪ��3NO2+H2O![]() 2HNO3+NO�����������̿�������������Ҫ�����������ԭ����___��
2HNO3+NO�����������̿�������������Ҫ�����������ԭ����___��
��5�����᳧��β�����е��������������ֱ���ŷŽ���Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H=��574kJ��mol��1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=��1160kJ��mol��1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ��___��