题目内容
(10分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g) CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
由表中数据判断ΔH1 0(填“>”、“=”或“<”)。
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为 。
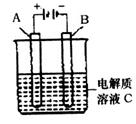
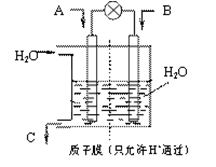
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
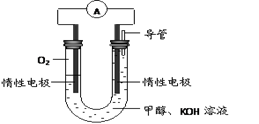
① 该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g)+2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1反应II:CO2(g)+3H2(g)
 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2①上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为 。
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

① 该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
(1)① I ②<③ 80%
(2)① O2 +2H2O +4e- = 4OH- ② 2CH3OH +3O2 +4OH-= 2CO32- + 6H2O
(2)① O2 +2H2O +4e- = 4OH- ② 2CH3OH +3O2 +4OH-= 2CO32- + 6H2O
(1)①根据反应式可知,反应I中反应物全部进入甲醇中,所以符合原子经济性原则。
②根据数据可知,随着温度的升高,平衡常数逐渐减小,说明升高温度,平衡向逆反应方向移动,因此正反应是放热反应。
③平衡时CO是0.2mol/L×2L=0.4mol,则消耗CO是2mol-0.4mol=1.6mol,所以CO的转化率是1.6÷2.0×100%=80%。
(2)①原电池中正极是得到电子的,所以氧气在正极通入,则正极反应式为O2 +2H2O +4e- = 4OH-。
②负极失去电子,即甲醇在负极通入,甲醇的氧化产物是碳酸钾,所以总反应式为2CH3OH +3O2 +4OH-= 2CO32- + 6H2O。
②根据数据可知,随着温度的升高,平衡常数逐渐减小,说明升高温度,平衡向逆反应方向移动,因此正反应是放热反应。
③平衡时CO是0.2mol/L×2L=0.4mol,则消耗CO是2mol-0.4mol=1.6mol,所以CO的转化率是1.6÷2.0×100%=80%。
(2)①原电池中正极是得到电子的,所以氧气在正极通入,则正极反应式为O2 +2H2O +4e- = 4OH-。
②负极失去电子,即甲醇在负极通入,甲醇的氧化产物是碳酸钾,所以总反应式为2CH3OH +3O2 +4OH-= 2CO32- + 6H2O。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 H2O(l) 的ΔH =" 40.69" kJ·mol-1
H2O(l) 的ΔH =" 40.69" kJ·mol-1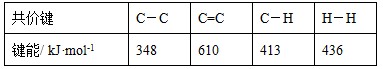
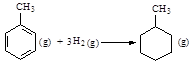 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1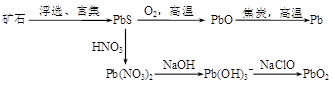
 N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol·L-1,
N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol·L-1,
 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变
2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 2OH?+H2↑+Cl2↑
2OH?+H2↑+Cl2↑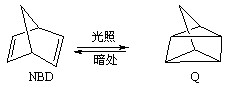 ,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高
,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高 2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1
2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1 (g)+
(g)+ 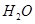 (g)=
(g)=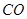 (g)+
(g)+ (g)
(g) 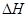 = +
= +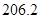
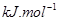
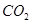 (g)=
(g)=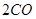 (g)+
(g)+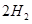 (g)
(g)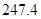
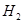 (g)的热化学方程式为 。
(g)的热化学方程式为 。 O的热分解也可得到H
O的热分解也可得到H